F-도핑된 탄소 코팅 고용량 Nano-Si 양극
F 도핑 탄소 코팅 고용량 나노-Si 양극: 기체 불소화 및 리튬 저장 성능
저자: SU Nan, QIU Jieshan, WANG Zhiyu. F 도핑 고용량 탄소 코팅 Nano-Si 양극: 기체 불소화에 의한 제조 및 리튬 저장 성능. 무기재료학회지, 2023, 38(8): 947-953 DOI:10.15541/jim20230009
초록
Si 양극은 고에너지 리튬 이온 개발에 엄청난 잠재력을 갖고 있습니다. 배터리. 그러나 Li 흡수에 따른 엄청난 양 변화로 인한 빠른 실패로 인해 Li 흡수가 방해됨 그들의 응용 프로그램. 이 연구는 간편하지만 독성이 낮은 가스 불소화를 보고합니다. F-도핑된 탄소 코팅 나노-Si 양극 재료를 생산하는 방법. 코팅 결함이 높은 F 도핑 탄소를 함유한 nano-Si는 Si를 효과적으로 보호할 수 있습니다. Li+ 운송을 촉진하면서 Li 저장 시 엄청난 양의 변화를 방지하고 안정적인 LiF가 풍부한 고체 전해질 간기(SEI) 형성. 이 양극은 다양한 용량에서 1540~580mAh·g-1의 고용량 0.2-5.0 A·g-1의 현재 비율을 유지하면서 200사이클 후 75% 용량. 이 방법은 또한 불소를 사용하는 전통적인 불소화 기술의 높은 비용과 독성 XeF2 및 F2와 같은 소스.
키워드ï¼ 리튬이온 배터리; Si 양극; F-도핑된 탄소; 기체 불소화 방법
효율적인 에너지 저장장치 개발 전환 기술은 '탄소 정점'이라는 목표를 달성하는 데 도움이 될 것입니다. 탄소 중립… 리튬이온 배터리는 현재 가장 널리 사용되는 배터리 중 하나입니다. 고효율 에너지 저장 기술을 사용했습니다 [1]. 그러나 상업적인 흑연 양극은 리튬 저장 용량이 낮아 리튬 저장 용량이 크게 제한됩니다. 리튬 이온 배터리의 에너지 밀도 [2]. 실리콘은 낮은 장점을 가지고 있습니다. 잠재적이고 풍부한 매장량과 이론적 특정 용량(4200 mAh·g-1)은 흑연계 음극에 비해 훨씬 높으므로 흑연을 대체할 음극재 후보 [3] 실리콘 소재 달성 리튬 이온과의 가역적 합금화 반응을 기반으로 한 리튬 저장, 하지만 이 과정에는 엄청난 양의 변화(~400%)가 수반되며, 이는 전극의 급격한 분말화 및 고장으로 인해 주요 병목 현상이 발생함 실리콘 음극의 실용화를 제한하고 있다[3-4].
최근 몇 년 동안 연구자들은 안정성과 전기화학적 특성을 향상시키기 위한 다양한 전략을 개발했습니다. 실리콘 양극의 성능. 예: 나노미터화[5], 구조적 전도성 탄소 및 기타 재료와의 복합 [6-7] 등 기계적 응력 완화를 통한 실리콘 양극의 구조적 안정성 현미경으로 볼 때 리튬 저장 공간의 부피 팽창과 관련이 있음 규모. 새로운 전해질 또는 전해질 첨가제를 개발하여 고체 전해질 계면 상의 안정성과 쿨롱 효율 (SEI) 실리콘 양극 [8]의 표면에. 효율적인 폴리머 개발 결합제(예: 카르복시메틸 셀룰로오스 나트륨, 알긴산 나트륨, 폴리아크릴 산성 기반 폴리로탁산[9] 등). 활성 물질 간의 결합력을 강화합니다. 재료, 활물질과 전도성 네트워크 사이, 전극막 및 집전체 [9-10]. 그 중 카본코팅이 하나인데요 실리콘 양극의 구조적 안정성을 향상시키는 가장 효과적인 수단 표면 및 인터페이스 속성을 변조합니다 [3-4,11]. 그러나, 단단히 코팅된 매우 안정적인 탄소층은 리튬 이온 이동을 방해하고 한계를 정합니다. 실리콘 양극의 전체 성능.
또한 반복되는 볼륨 연속 충방전 과정에서 실리콘 양극의 변화 또한 SEI 필름이 지속적으로 파손되고 반복적으로 성장하여 결과적으로 전극 표면의 활성 리튬과 전해질의 지속적인 손실 [12]. 위와 같은 문제점에 대해 본 연구에서는 효율적인 방법을 제안한다. 실리콘 음극재 표면을 코팅하는 기상 불소화 방식 불소 원소가 풍부한 결함이 많은 비정질 탄소층을 사용하여 구조와 인터페이스 안정성을 향상시킵니다. 전통적인 것과 비교하여 고비용, 독성이 강한 불소원을 이용한 불소화 기술 XeF2 또는 F2[13]와 같은 이 전략은 더 간단하고 독성이 적습니다. 그만큼 나노실리콘 소재 표면에 불소를 첨가한 탄소층을 코팅해 리튬 내장 실리콘 양극의 부피 팽창을 효과적으로 완충 리튬 이온 수송 능력을 향상시키는 동시에. 그리고 매우 안정적인 SEI 무기 불소가 풍부한 필름은 다음과 같은 목표를 달성하기 위해 현장에서 제작됩니다. 실리콘 양극의 사이클 안정성을 향상시킨다.
1 실험방법
1.1 재료준비
카본 코팅의 제조 나노실리콘(Si@C):상업용 나노실리카 0.3g 분말(입자 크기 20~100nm, 알라딘 시약)을 초음파로 탈이온수와 에탄올의 혼합용매 28mL에 분산시켰다(부피). 비율 5:2). 3-아미노프로필트리에톡시실란 0.4 mL를 첨가한 후 2시간 동안 저어줍니다. 균일한 분산액을 형성하기 위해 A. 4,4-디하이드록시디페닐 0.115g을 녹인다. 탈이온 혼합용매 28 mL에 황화물과 3-아미노페놀 0.1 g을 첨가한 용액 물과 에탄올(부피비 5:2)을 혼합하여 균일한 용액을 만듭니다. B. 혼합합니다. 분산액 A와 용액 B를 균일하게 섞은 후 암모니아수 0.1mL를 첨가하고 30분 동안 저어줍니다. 그런 다음 0.14 mL 포름알데히드 용액(37%~40%)을 첨가하고 일정하게 반응합니다. 30°C에서 12시간 동안 교반하였다. 반응 후 페놀수지로 코팅된 나노실리카(Si@AF)는 원심분리하고 에탄올로 세척하여 얻었으며 탈이온수를 3회 교대로 사용합니다. 800°C의 아르곤 가스에서 하소되었습니다. 3시간 동안 탄소 코팅된 나노실리콘(Si@C)을 얻는다.
불소 도핑의 제조 탄소 코팅 나노 실리콘(Si@C-F): 100 mg Si@C 및 200 mg 폴리비닐리덴 플루오라이드(PVDF)를 아르곤 보호 튜브 퍼니스에 넣었습니다. PVDF가 포함된 석영 보트는 공기 흐름의 상류에 위치하며, Si@C가 포함된 석영 보트는 공기 흐름의 하류에 위치합니다. 구운 것입니다 600°C에서 3시간 동안 불소가 도핑된 탄소 코팅 나노실리콘(Si@C-F)을 얻습니다.
1.2 배터리 조립 및 전기화학적 성능시험
1.2.1 배터리 조립
CR2016 버튼 배터리 조립 테스트용. 활물질과 전도성 카본블랙을 혼합하고 카르복시메틸셀룰로오스 나트륨 결합제를 7:2:1의 질량비로 균일하게 혼합합니다. 탈이온화 용매 및 분산제로 물을 첨가하여 얻은 슬러리를 얻었다. 동박 위에 균일하게 코팅하여 작업전극으로 사용합니다. 활성 물질 로딩은 0.8~1.0 mg·cm-2였습니다. 금속 리튬 시트가 카운터로 사용되었습니다. 전극 및 기준 전극. 전해질은 DOL/DME 용액입니다. 1.0 mol/L LiTFSI(리튬 비스트리플루오로메탄설포네이트 이미드)에 용해되고 2.0% LiNO3(DOL은 1,3-디옥솔란, DME는 에틸렌 글리콜 디메틸 에테르, 부피 비율 1:1). 아르곤으로 채워진 글러브 박스(수분 함량 < 0.1 μL/L, 산소 함량 < 0.1 μL/L)에 셀을 조립합니다.
1.2.2 배터리 성능 테스트
IVIUM Vertex.C.EIS 전기화학적 사용 반응 메커니즘과 반응 동역학을 분석하는 워크스테이션 CV(Cyclic Voltammetry) 방식을 사용하는 배터리입니다. 전압 범위는 0.01~1.5입니다. V, 스위프 속도는 0.05~0.5mV·s-입니다. 1. 전기화학적 임피던스 분광학(EIS)을 사용하여 전극 역학을 분석했습니다. 테스트 주파수 범위는 100kHz~10mHz이고, 방해 전압 진폭은 5.0mV이다. Land CT2001A 배터리 테스터는 리튬 저장 성능을 연구하는 데 사용되었습니다. 정전류 충전 및 방전 방식을 사용합니다. 전압 창은 0.01~1.5V(vs. Li/Li+), 전류밀도는 0.2~5.0A·g-1이었다.
2 결과 및 논의
2.1 재료의 외관, 구조 및 조성 분석
준비 과정 불소가 첨가된 탄소 코팅 나노 실리콘 소재는 그림 1에 나와 있습니다. 먼저, 폴리머 코팅된 실리콘 나노입자(Si@AF)를 기반으로 준비합니다. 페놀-알데히드 축합중합 반응으로 전환됩니다. 고온에서 비정질 탄소 코팅 나노실리콘 나노입자(Si@C). 그 다음에 폴리비닐리덴 플루오라이드를 불소 공급원으로 사용하고 불소를 도핑합니다. 기상을 통해 실리콘 나노입자 외부의 탄소층으로 고온에서 불소화 방법. 그림 2(a)는 의 XRD 패턴을 보여줍니다. Si@C 및 Si@C-F 재료. 2θ=28°, 47°, 56°, 69°에 위치한 회절 피크 그리고 76°. (111), (220), (311), (400) 및 (331) 결정에 해당합니다. 단결정 실리콘 평면(JCPDS 77-2108). 넓은 봉우리가 위치한 2θ=25°~26°에서 형성된 단거리 정렬 탄소 구조에 기인합니다. 페놀 축중합 생성물의 탄화에 의한 것. 그만큼 높은 전도성과 우수한 구조적 유연성을 지닌 카본 코팅층 실리콘 재료의 분쇄 실패를 효과적으로 완화할 수 있습니다. 충전 및 방전 과정을 개선하고 전극의 전도성을 향상시킵니다. 그림 2(b)는 Si@C 및 Si@C-F 재료의 라만 스펙트럼입니다. 흡수 피크는 515, 947, 1350 및 1594cm-1에 나타납니다. 그 중에는 515와 947cm-1의 흡수 피크는 다음의 특징적인 피크입니다. 1차 광포논에서 파생된 결정질 실리콘 실리콘의 산란 및 2차 횡방향 광포논 산란 각각 [14]. 1350 및 1594cm-1의 흡수 피크는 다음과 같습니다. 방향족 탄소 구성 신축 진동(G 모드) 및 무질서 결함 탄소 구조(D 모드). 일반적으로 말해서, D 모드와 G 모드의 강도 비율(ID/IG)을 사용하여 정도를 측정할 수 있습니다. 탄소 재료의 결함 및 무질서 [15]. Si@C 소재와 비교 (ID/IG=0.99), Si@C-F 재료의 ID/IG는 1.08로 증가합니다. 이는 불소화 공정은 탄소 코팅층의 결함을 증가시킬 수 있으며, 나노실리콘을 촘촘하게 코팅하면서 리튬이온을 향상시키는데 도움이 되는 제품입니다. 운송 능력.
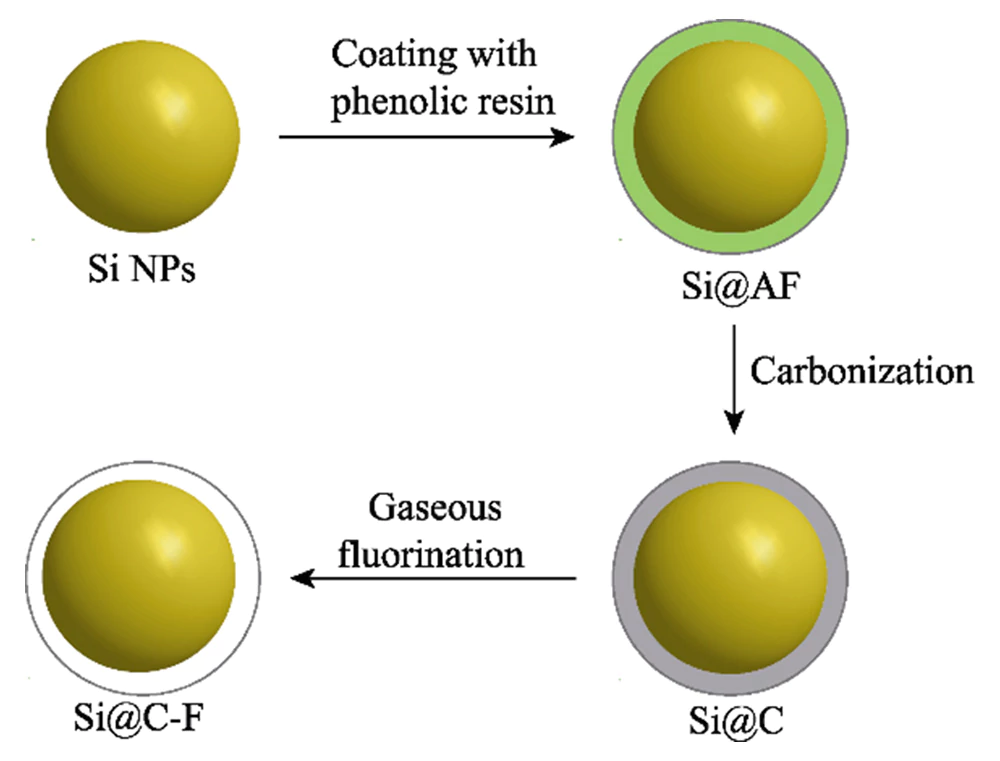
그림. 1 Si@C-F 생산의 개략도
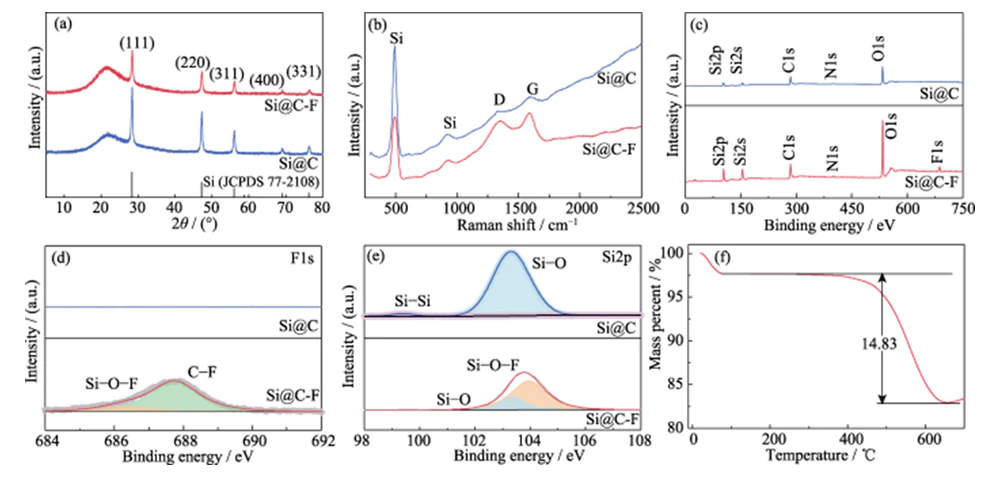
그림. 2 (a) XRD 패턴, (b) 라만 스펙트럼, (c) XPS 측량 스캔, (d) 고해상도 F1 및 (e) Si@C의 Si2p XPS 스펙트럼 및 Si@C-F, (f) Si@C-F의 TGA 곡선
XPS 전체 스펙트럼은 Si@C 재료에는 O, N, C 및 Si 원소가 포함되어 있습니다(그림 2(c)). 원자 불소화 후 얻은 Si@C-F 재료의 F 원소 분율 처리율은 약 1.8%이다. 고해상도 F1s XPS 스펙트럼 (그림 2(d)), 결합 에너지 686.3에서 두 개의 특징적인 피크와 687.8 eV는 각각 C-F 및 Si-O-F에 해당하며 C-F가 지배적입니다. 하나. 불소화 처리가 성공적으로 불소를 도입했음을 보여줍니다. 나노 실리콘 표면에 코팅된 비정질 탄소층에 원소를 삽입합니다. 그만큼 고해상도 Si2p(그림 2(e))와 F1s XPS 스펙트럼은 Si 원자가 Si-O-F를 형성하여 탄소층의 F 원소와 화학적으로 상호작용합니다. 이는 탄소층을 촘촘하게 코팅하는 데 유리합니다. 실리콘 표면. 열중량 분석(TGA)은 질량 분율이 Si@C-F 재료에서 Si의 비율은 약 85.17%입니다(그림 2(f)).
SEM 분석에 따르면 Si@C-F 재료는 <100nm 크기의 나노입자로 구성됩니다(그림 3(a~c)). 고온 탄화 및 기상 불소화 처리 후에도 실리콘 나노입자 표면에는 여전히 탄소재료가 균일하게 코팅되어 있다.
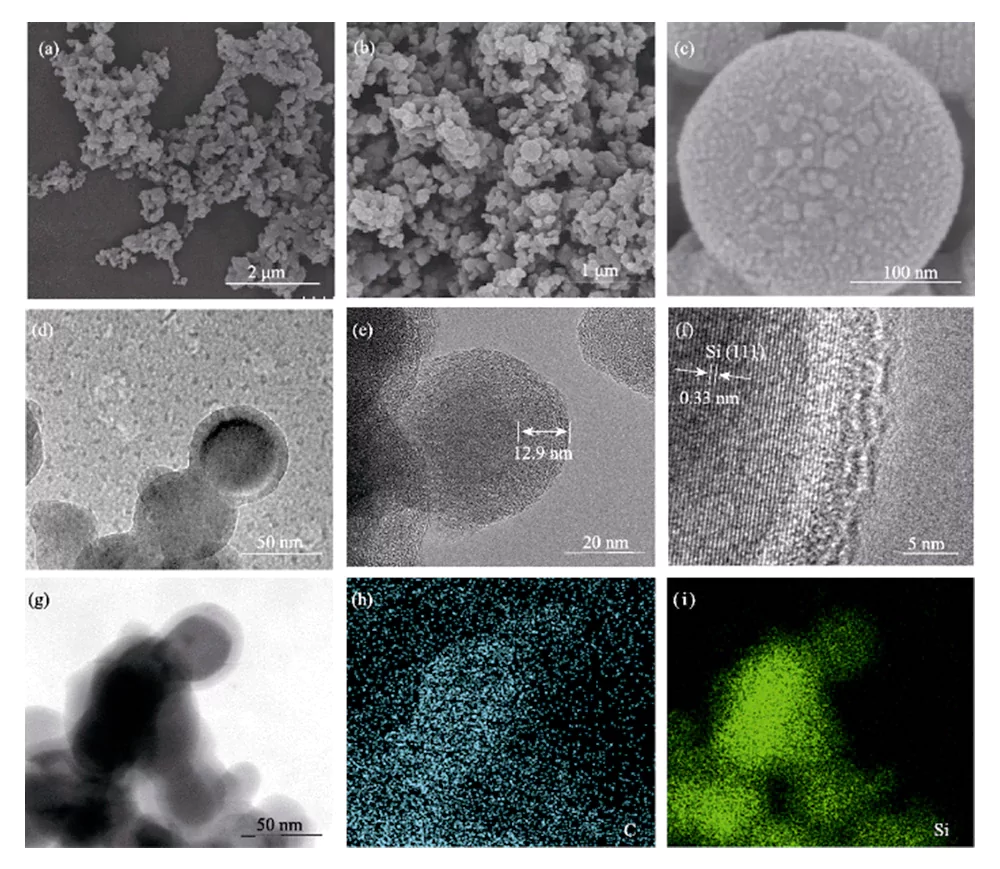
그림. 3 (a-c) SEM 이미지, (d-f) TEM 이미지 및 (g-i) Si@C-F의 원소 매핑
TEM 분석에 따르면 실리콘은 나노입자는 탄소층에 완전하고 균일하게 코팅되어 있습니다. 약 10나노미터의 두께로 코어-쉘 구조를 형성합니다(그림 3(d~e)). 실리콘 나노입자는 단결정 구조를 가지고 있으며, 0.328nm의 격자 간격은 Si의 (111) 결정면에 해당하며, 이를 덮고 있는 불소 도핑 탄소층은 비정질 구조를 가지고 있습니다(그림 3(f)). 원소 분포 스펙트럼은 C 및 Si 원소가 Si@C-F에 고르게 분포되어 있다(그림 3(g~i)).
2.2 전기화학적 성질 재료
그림 4(a, b)는 Si@C와 Si@C-F 양극재의 CV 곡선이다. 스위프 속도는 0.1mV·s-1이고 전압 범위는 0.01~1.5V입니다. 사이클에서 0.1~0.4V 범위의 약하고 넓은 피크는 SEI 필름을 형성하기 위한 비가역적인 전해질 분해 과정; 그만큼 0.01V에서의 감소 피크는 결정질 실리콘 공정에 해당합니다. 합금 반응을 통해 실리콘-리튬 합금(LixSi)을 형성합니다. 후속하는 동안 충전 과정에서 0.32 및 0.49 V의 두 산화 피크는 비정질 실리콘을 형성하기 위한 LixSi의 탈합금 공정 [16]. 불소화 처리는 구조적 도핑 및 에칭 효과를 얻을 수 있습니다. 다수의 구조적 결함은 코팅된 비정질 탄소층에 유입됩니다. 3차원 리튬 이온 수송을 형성하는 Si 재료의 표면 채널, 리튬 이온 수송을 가속화하고 전기 화학을 향상시킵니다. Si 재료의 반응성. 따라서 Si@C-F는 더 날카로운 특성을 나타냅니다. 불소가 없는 Si@C 양극보다 0.49V에서 탈리튬화 산화 피크 도핑. 후속 방전 과정에서 새로운 감소 피크는 0.19입니다. V는 형성된 비정질 실리콘의 리튬 삽입 과정에 해당합니다. 첫 번째 충전 과정에서 [16-17]. 사이클 수가 증가함에 따라, CV 곡선에서 산화 피크와 환원 피크의 위치 더 긴 변화는 Si@C 및 Si@C-F 양극 재료가 유사한 방식을 따른다는 것을 나타냅니다. 첫 번째 충전 및 방전 후 합금 리튬 저장 메커니즘. 동안 이 과정에서 산화피크와 환원피크가 점차 증가하고, 일반적인 전극 활성화 과정을 반영합니다.
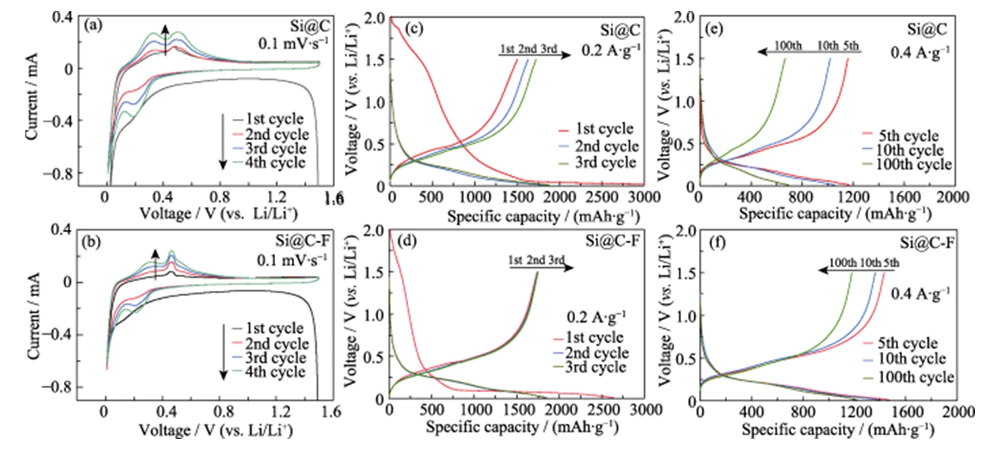
그림. 4 (a, b) (a, c, e) Si@C 및 (b, d, f) Si@C-F 양극
정전류 충전과 방전 테스트에서 Si 양극 재료는 한 번에 4회 순환되고 활성화되었습니다. 더 낮은 전류 밀도(0.2 A·g-1)로 사이클 안정성을 테스트했습니다. 0.4 A·g-1의 전류 밀도. 그림 4 (c, d)는 정전류 전하를 보여줍니다. 0.2 A·g-1에서 Si@C 및 Si@C-F 양극의 방전 곡선 및 전압 창은 0.01~1.5V입니다. 첫 번째 방전 과정에서 둘 다 긴 모양을 형성했습니다. 결정질 실리콘 합금의 리튬 삽입 공정에 해당하는 전압 범위 <0.1V의 플랫폼. 이 과정은 종종 낮은 1차 쿨롱 효율을 동반합니다. 첫 번째 충전 과정에서 실리콘-리튬 합금은 탈리튬화되어 리튬 삽입을 위한 활성화 에너지가 낮은 비정질 실리콘으로 변환되며[18], 첫 번째 충방전 후 리튬 삽입 전위가 0.1~0.3V로 증가합니다. Si@C와 비교하여 Si@C-F 양극의 첫 번째 방전 비용량(2640mAh·g-1)은 약간 낮습니다. 그러나 1차 충전 비용량(1739.6 mAh·g-1)은 Si@C 양극에 비해 더 높고, 1차 쿨롱 효율(65.9%)은 약 45.8% 더 높다. Si@C-F 음극의 SEI 영역의 충방전 곡선은 Si@C의 충방전 곡선보다 짧아 표면에 보다 안정적인 SEI 피막이 형성되었음을 나타냅니다. 이는 불소가 도핑된 탄소층이 무기 성분(예: LiF)을 함유한 SEI 필름의 형성을 유도하고 실리콘 양극 표면의 안정성을 높여 비가역적인 리튬 손실과 전해질 소비를 줄이는 데 도움이 되기 때문입니다.
그림 4(e~f)는 Si@C의 충전 및 방전 곡선을 보여줍니다. 활성화 후 전류 밀도 0.4 A·g-1의 Si@C-F 음극. 100사이클 후에도 Si@C-F 양극은 여전히 높은 비용량을 유지할 수 있습니다. 1223mAh·g-1이며 용량 유지율이 85%를 초과합니다(그림 5(a)). 아래에 동일한 조건에서 Si@C 음극의 용량은 불소화 처리는 충방전 과정에서 급격하게 쇠퇴하고, 100사이클 후 용량 유지율은 62%에 불과했습니다. 그것은 다음을 보여줍니다 불소가 도핑된 탄소 코팅층은 성능 향상에 큰 영향을 미칩니다. 실리콘 양극의 주기 안정성. 광고 탄소 코팅이 없는 나노 실리콘 양극은 10회 이상의 주기 후에 실패합니다. 엄청난 부피 팽창과 구조적 파우더링으로 인해 리튬의 탈삽입. 이 과정에서 특정 용량의 Si@C-F 및 Si@C 음극은 처음 10~20년 동안 점차 증가합니다. 활성화 효과로 인한 순환. 0.2~5.0의 큰 전류밀도에서 A·g-1, Si@C-F 양극은 1540~580의 높은 비용량을 유지할 수 있습니다. mAh·g-1, 우수한 용량 유지율을 보여줍니다(그림 5(b)). 고전류에서 밀도가 5.0A·g-1로 용량 유지율이 약 78% 더 높습니다. Si@C보다요. 전류밀도를 0.2A·g-1로 더 낮추면, 특정 용량은 1450mAh·g-1로 복원될 수 있으며 이는 구조는 고속 리튬 저장 중에 매우 안정적입니다. 200 이후 0.2 A·g-1의 전류 밀도에서 충방전 주기를 갖는 Si@C-F 양극은 75%의 특정 용량을 유지합니다. 용량 유지율 불소화 처리가 없는 Si@C 양극은 40%에 불과합니다(그림 5(c)). 이 양극 또한 실리콘 양극 소재보다 더 나은 리튬 저장 성능을 나타냅니다. 문헌에 보고되어 있다(표 1).
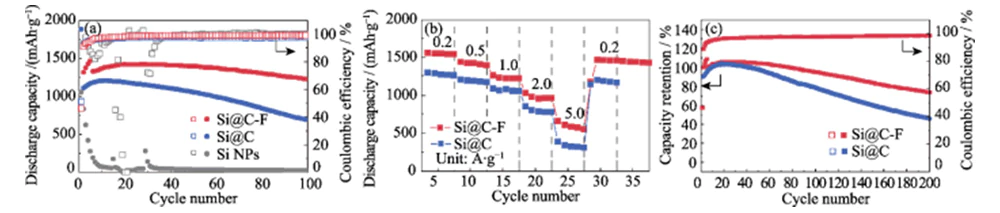
그림. 5 (a) 전류 밀도 0.4에서의 사이클링 안정성 4로 활성화된 양극이 있는 A·g-1 사이클링 전 0.2A·g-1에서 사이클, (b) 다양한 전류 밀도에서의 속도 성능 0.2~5.0 A·g·1 범위 및 (c) Si@C 및 Si@C-F 양극의 리튬 저장을 위해 0.2 A·g-1 전류 밀도에서 용량 유지
표 1 Si@C-F 양극과 Si@C-F의 비교 Si 기반 음극의 전기화학적 성능 보고
|
재료 |
초기 CE |
초기용량/(mAh·g-1) |
용량유지 |
참고 |
|
Si@C-F |
65.9% |
2640 |
85%(100사이클) |
이 작품 |
|
나노-Si/TiN@ |
71% |
2716 |
59.4% (110주기) |
[20] |
|
Si@C@RGO |
74.5% |
1474 |
48.9%(40사이클) |
[21] |
|
시@FA |
65% |
1334 |
68.7%(100주기) |
[22] |
|
p-Si@C |
58% |
3460 |
57.5%(100주기) |
[23] |
|
Si@void@C |
- |
900 |
70%(100사이클) |
[24] |
|
실리콘/C@C |
- |
1120 |
80%(100사이클) |
[25] |
고전류에서 밀도가 5.0A·g-1로 용량 유지율이 약 78% 더 높습니다. Si@C보다요. 전류밀도를 0.2A·g-1로 더 낮추면, 특정 용량은 1450mAh·g-1로 복원될 수 있으며 이는 구조는 고속 리튬 저장 중에 매우 안정적입니다. 200 이후 0.2 A·g-1의 전류 밀도에서 충방전 주기를 갖는 Si@C-F 양극은 75%의 특정 용량을 유지합니다. 용량 유지율 불소화 처리가 없는 Si@C 양극은 40%에 불과합니다(그림 5(c)). 이 양극 또한 실리콘 양극 소재보다 더 나은 리튬 저장 성능을 나타냅니다. 문헌에 보고되어 있습니다(표 1). 코팅 내 불소 도핑량 탄소층은 리튬 저장 성능에 큰 영향을 미칩니다. Si@C-F 양극. 불소 도핑량이 원자 분율 1.8% 미만인 경우, Si@C-F 양극의 순환 안정성은 다음과 같이 크게 향상됩니다. 불소 도핑량이 증가합니다(그림 6). 강화된 효과 때문이에요 탄소의 리튬 이온 수송 특성에 대한 불소 도핑 실리콘 표면의 코팅층과 SEI 필름의 안정성 재료. 불소 도핑 비율이 너무 높은 경우(2.7%), 탄소 코팅 Si 양극재는 여전히 양호한 사이클 안정성을 유지하지만 특정 용량이 크게 떨어집니다. 이는 활성 Si의 손실로 인한 것입니다. 고온 중 기상 불소종 에칭으로 인해 발생 불소화. 불소 도핑량이 1.8원자%일 때 Si@C-F는 양극은 최적의 사이클 안정성과 높은 비용량을 나타냅니다.
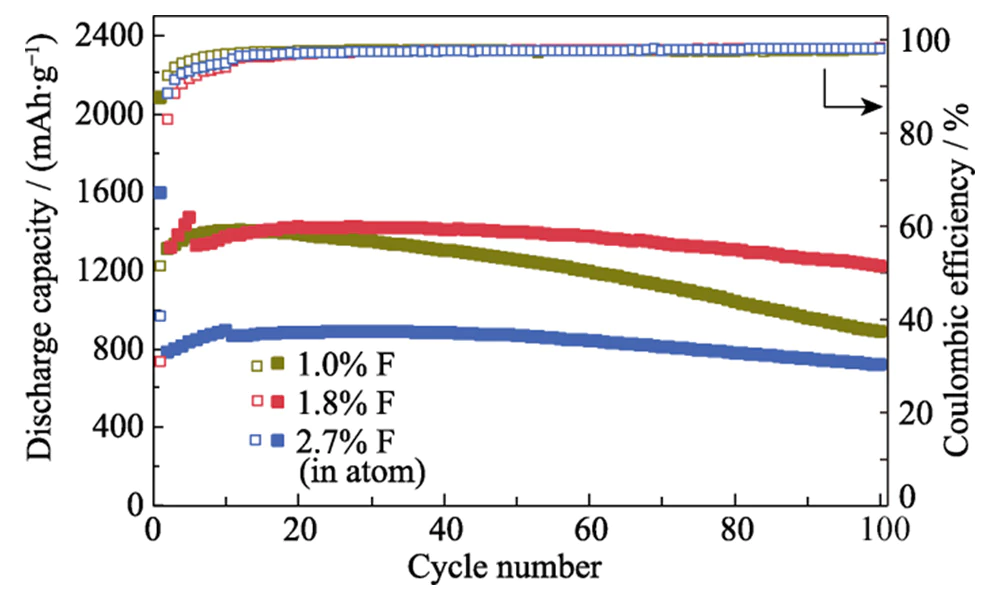
그림. 6 다양한 Si@C-F 양극의 순환 안정성 사이클링 전 0.2 A·g-1에서 4~10주기로 활성화된 양극을 사용하여 전류 밀도 0.4 A·g-1에서의 F 비율
Si@C 및 Si@C-F의 EIS 스펙트럼 양극은 중~고주파 영역의 반호 곡선으로 구성되며, 저주파 영역에서 기울어진 직선(그림 7(a)). 세미 아크 중~고주파 범위의 곡선은 전하 이동과 관련이 있습니다. 저항(Rct), 저주파 범위의 기울어진 직선 주로 리튬 이온 확산의 Warburg 임피던스(ZW)를 반영합니다[26]. 충전 및 방전 전, Si@C-F 및 Si@C 음극의 Rct 유사하지만 전자는 불량률이 높아 ZW가 낮습니다. 표면을 덮고 있는 불소 첨가 탄소층. 충전 및 방전 후 사이클에서 Si@C-F 양극의 Rct(5.51 Λ)는 그보다 훨씬 낮습니다. Si@C 양극(21.97 Ω)(그림 7(b))의 ZW는 훨씬 낮습니다. 후자. 이는 불소가 풍부한 SEI 인터페이스 필름이 유도된 것을 보여줍니다. 불소 첨가 탄소층은 계면 전하를 효과적으로 향상시킬 수 있으며 리튬 이온 수송 능력.
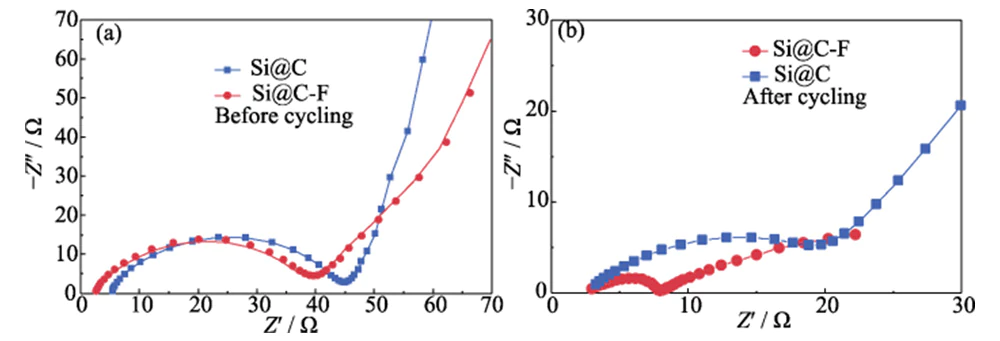
그림 7 Si@C 및 Si@C-F 양극의 나이퀴스트 플롯(a) (b) 전류 밀도 0.4 A·g-1에서 사이클링 전과 후
2.3 충방전 후 전극구조의 특성
충전 및 방전 후 SEM 특성화 사이클(그림 8(a~c))은 상당한 부피 팽창으로 인해 리튬 삽입 과정에서 실리콘의 영향, 두께 Si@C 전극은 132.3% 증가했습니다. 이는 전달을 방해할 뿐만 아니라 이온과 전자는 내부 저항과 분극을 증가시킵니다. 전극은 또한 큰 기계적 응력을 유발하여 전극이 파열되어 집전체에서 분리되어 성능이 저하됩니다. Si@C 양극은 빠르게 붕괴됩니다(그림 5(c)). 이에 비해 전극은 Si@C-F 양극의 두께는 충전 후 26.6%만 증가했으며, 방전 사이클을 유지하고 우수한 전극 구조적 안정성을 유지했습니다(그림 8(d~f)). 이는 도입된 불소 도핑 탄소층이 실리콘에 리튬 삽입으로 인한 부피 팽창 효과를 효과적으로 완충 마이크로 스케일의 재료를 사용하여 구조적 안정성을 향상시킵니다. 거시적 규모의 전극을 아래에서 위로.
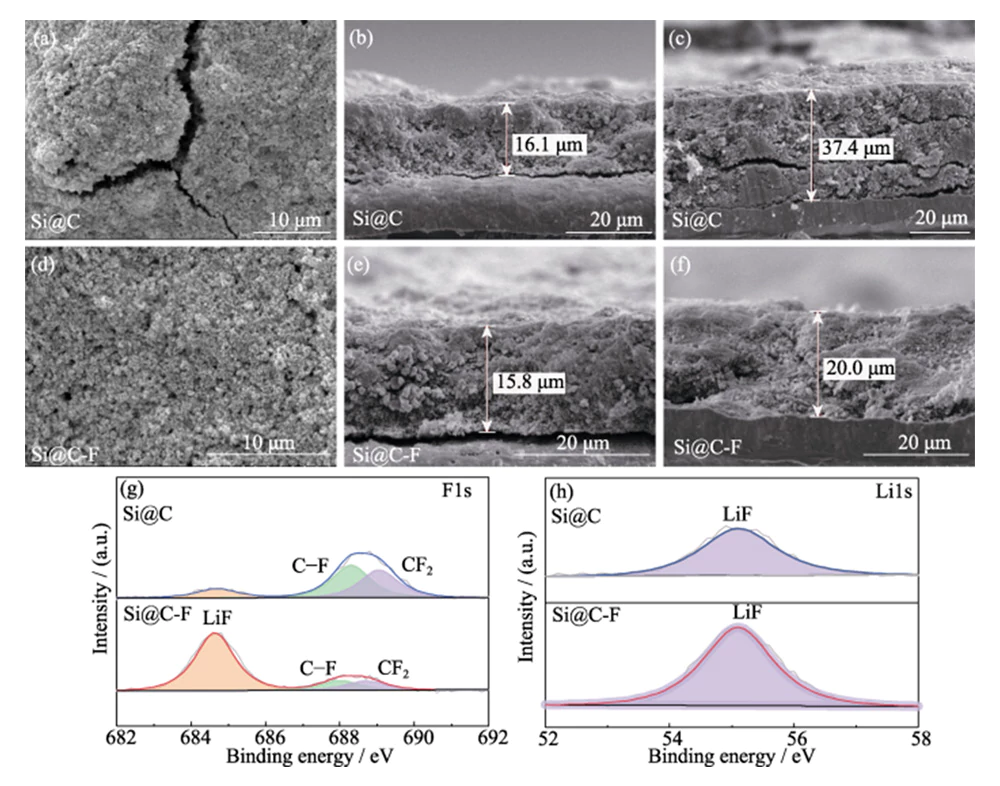
그림 8 (a) Si@C 및 (d) Si@C-F 양극의 상위 SEM 이미지 사이클링 후; (b, c) Si@C 및 (e, f) Si@C-F 양극의 단면 SEM 이미지 (b, e) 사이클링 전과 (c, f) 사이클링 후; 고해상도 (g) F1 및 (h) Li1 사이클링 후 Si@C 및 Si@C-F 양극에 대한 SEI의 XPS 스펙트럼
Si@C 표면의 SEI 필름 구성 및 충방전 사이클 후 Si@C-F 음극을 분석했습니다. XPS 기준(그림 8(g~h)). 고해상도 F1s XPS 스펙트럼에서 바인딩 684.8, 688.3 및 689.1eV의 결합 에너지에서 에너지 피크는 해당합니다. LiF, CF 결합 및 CF2에 각각 적용됩니다. 이에 맞춰 다음도 있습니다. 고해상도 Li1s의 LiF 종에 해당하는 특성 피크 XPS 스펙트럼은 LiF 종을 포함하는 SEI 필름이 형성되었음을 나타냅니다. 실리콘 양극의 표면. Si@C 양극과 비교하여 LiF 함량은 Si@C-F 양극 표면의 LiF가 더 높다는 것을 나타냅니다. SEI 필름은 리튬염의 분해뿐만 아니라 전해질뿐만 아니라 불소가 도핑된 탄소층의 F로부터도 발생합니다. 그만큼 고탄성 LiF의 형성은 구조적 강도를 효과적으로 증가시킬 수 있습니다 SEI 필름의 실리콘 내 리튬 삽입의 부피 변화를 억제합니다. 재료. 동시에 LiF의 넓은 밴드갭과 절연 특성 SEI 두께를 줄이고 초기 비가역적 리튬 손실을 줄일 수 있습니다. LiF와 Si의 리튬화 생성물인 LixSi 합금은 높은 계면을 가지고 있습니다. 에너지를 공급하고 리튬화된 실리콘의 소성 변형에 더 잘 적응할 수 있습니다. 사이클링 중 양극으로 인해 사이클링 안정성이 더욱 향상됩니다. 전극 [19].
3 결론
본 연구에서는 불소가 도핑된 탄소 코팅 나노 실리콘 소재는 간단한 방법을 통해 제조되었습니다. 저독성 기상 불소화 방법. 연구에 따르면 불소 도핑은 (1.8% F)는 한편으로는 탄소 코팅층의 결함을 증가시킵니다. 실리콘 표면은 풍부한 리튬 이온 수송 채널을 제공하는 동시에 나노 실리콘을 촘촘하게 코팅하여 부피 팽창을 억제합니다. 다른 한편으로는 LiF가 풍부한 매우 안정적인 SEI 필름이 표면에 유도됩니다. 나노 실리콘 소재로 안정성과 쿨롱 효율을 더욱 향상시켰습니다. 실리콘 양극의. 덕분에 최초로 쿨롱 효율을 얻었습니다. 불소가 첨가된 탄소 코팅 나노실리콘 양극은 65.9%로 향상되었습니다. 현재 밀도는 0.2~5.0 A·g-1로 1540~580의 높은 비용량을 나타냅니다. mAh·g-1이며 200사이클 후에도 초기 용량의 75%를 유지할 수 있습니다. 이 연구는 실리콘 양극의 설계 및 구성에 대한 새로운 아이디어를 제공합니다. 고용량, 높은 안정성을 지닌 소재입니다.
참고자료
[1] NIU S S, WANG Z Y, YU M L 등MXene 기반 강화된 의사 용량 및 전력용 체적 용량을 갖춘 전극 유형 및 초장기 리튬 저장 장치.ACS Nano, 2018, 12(4): 3928.
[2] SU X, WU Q L, LI J C, et al.실리콘 기반 나노물질 리튬 이온 배터리: 검토.Advanced Energy Materials, 2014, 4(1): 1300882.
[3] GE M Z, CAO CY, GILL MB 등 최근 발전 실리콘 기반 전극: 기초 연구부터 실용화까지 응용 분야.Advanced Materials, 2021, 33(16): 2004577.
[4] LI P, ZHAO G Q, ZHENG X B, 외. 실리콘 기반의 최근 진행 상황 실용적인 리튬이온 배터리 응용을 위한 양극 소재.에너지 보관 재료, 2018, 15: 422.
[5] 리우 X H, ZHONG L, HUANG S 외 크기에 따라 다름 리튬화 중 실리콘 나노입자의 파손.ACS Nano, 2012, 6(2): 1522.
[6] 루오 W, 왕 Y X, CHOU S L 등 페놀의 임계 두께 장기 사이클 안정성 향상을 위한 수지 기반 탄소 계면층 실리콘 나노입자 양극.Nano Energy, 2016, 27: 255.
[7] DOU F, SHI L Y, CHEN G R, 실리콘/탄소 복합 음극재 리튬 이온 배터리.전기화학 에너지 리뷰, 2019, 2(1): 149.
[8] 지아H P, ZOU L F, GAO P Y 외 고성능 불연성 국부적 고농도화로 구현된 실리콘 양극 전해질.Advanced Energy Materials, 2019, 9(31): 1900784.
[9] 최스 H, KWON T W, COSKUN A 등고탄성 리튬에 실리콘 미세입자 양극용 폴리로탁산을 통합한 바인더 이온 배터리.Science, 2017, 357: 279.
[10] 리즈 H, ZHANG Y P, LIU T F 외 실리콘 양극 변조된 삼관능성 바인더를 통해 높은 초기 쿨롱 효율을 제공합니다. 대용량 리튬 이온 배터리.고급 에너지 자료, 2020, 10(20): 1903110.
[11] XU Z L, CAO K, ABOUALI S 등 al.고성능 탄소 코팅 Si의 리튬화 메커니즘 연구 현장 현미경에 의한 양극. 에너지 저장 재료, 2016, 3: 45.
[12] 테키R,모니K D, RAHUL K, 외.나노구조 실리콘 양극 리튬 이온 충전지.소형, 2009, 5(20): 2236.
[13] 시아에스 X, ZHANG X, LUO L L, 외.매우 안정적임 및 불소화 탄소 섬유로 구현된 초고속 리튬 금속 양극. Small, 2021, 17: 2006002.
[14] 장스 L, WANG X, HO K S 등 라만 스펙트럼 p형 다공성 실리콘의 넓은 주파수 영역.Journal of Applied 물리학, 1994, 76(5): 3016.
[15] 황W, 왕Y, 루오G H, et al.99.9% 진공에 의한 순도 다중벽 탄소 나노튜브 고온 어닐링 .Carbon, 2003, 41(13): 2585.
[16] 맥도웰M T, LEE S W, NIX W D 외 25주년 기사: 실리콘 및 기타 합금 양극의 리튬화 이해 리튬 이온 배터리.Advanced Materials, 2013, 25(36): 4966.
[17] 키 B, MORCRETTE M, TARASCON J 실리콘의 M.Pair 분포 함수 분석 및 고체 NMR 연구 리튬 이온 배터리용 전극: (탈)리튬화의 이해 메커니즘 .Journal of American Chemical Society, 2011, 133(3): 503.
[18] 가오H, 샤오엘 S, PLUMEL I, et al.나노 크기의 기생 반응 리튬 이온 배터리용 실리콘 양극.Nano Letters, 2017, 17(3): 1512.
[19] 첸제이, 팬엑스 L, LI Q, 외.LiF가 풍부한 전해질 설계 고성능 마이크로 크기 합금 양극을 가능하게 하는 고체 전해질 인터페이스 배터리용.Nature Energy, 2020, 5(5): 386.
[20] 장피, 가오와이 Q, RU Q, et al.다공성 물질의 확장 가능한 준비 리튬이온 배터리용 나노실리콘/TiN@탄소 양극.적용 표면 과학, 2019, 498: 143829.
[21] SU M R, WAN H F, LIU Y J 외 다층 리튬 이온 배터리용 양극으로 사용되는 탄소 코팅 Si 기반 복합재.분말 기술, 2018, 323: 294.
[22] PU J B, QIN J, 왕 Y Z, et al.마이크로 나노구 구조의 합성 리튬 이온 배터리용 양극 재료로 사용되는 실리콘-탄소 복합재.화학 물리학 편지, 2022, 806: 140006.
[23] 가오R S, TANG J, YU X L, 외 샌드위치형 실리콘-탄소 리튬이온의 신속한 저장을 위해 표면중합을 통해 제조된 복합체.
나노 에너지, 2020, 70: 104444.
[24] 공엑스 H, ZHENG Y B, ZHENG J 등 노른자 껍질 알루미늄-실리콘 합금을 양극으로 사용하여 제조된 실리콘/탄소 복합재 리튬이온 배터리용 재료.Ionics, 2021, 27: 1939.
[25] 리아와이 R, WANG R Y, ZHANG J W 외 샌드위치 리튬이온용 탄소코팅 실리콘/탄소나노섬유 음극 구조 배터리.Ceramics International, 2019, 45: 16195.
[26] YANG X M AND ROGACH A L.배터리 연구의 전기화학 기술: 튜토리얼 nonelectrochemists.Advanced Energy Materials, 2019, 9(25): 1900747.



