전고체박막 리튬전지용 비정질 LiSiON 박막전해질
저자: XIA Qiuying, SUN Shuo, ZAN Feng, XU Jing, XIA Hui
재료학부 난징 과학기술대학교 과학공학과, 난징 210094, 중국
초록
전고체박막리튬전지(TFLB)가 최적의 배터리로 꼽힌다. 마이크로 전자 장치의 전원. 그러나 상대적으로 낮은 이온 비정질 고체 전해질의 전도도는 전도성 향상을 제한합니다. TFLB의 전기화학적 성능. 이번 연구에서는 비정질 리튬실리콘 마그네트론 스퍼터링을 통해 산질화물(LiSiON) 박막을 제조합니다. TFLB용 고체전해질. 최적화된 증착 조건으로 LiSiON 박막은 실내에서 6.3×10-6 S…cm-1의 높은 이온 전도도를 나타냅니다. 온도와 5V 이상의 넓은 전압 범위로 적합한 박막이 됩니다. TFLB용 전해질. MoO3/LiSiON/Li TFLB는 큰 특성을 지닌 LiSiON 박막 전해질을 기반으로 제작되었습니다. 용량(50mA...g-1에서 282mAh...g-1), 양호한 속도 용량(800mA...g-1에서 50mAh...g-1), 허용 가능 사이클 수명(200사이클 후 78.1% 용량 유지)을 입증합니다. 실제 적용을 위한 이 전해질의 타당성
키워드 ï¼ LiSiON; 얇은 필름 전해질; 전고체 리튬 배터리; 박막전지
다음과 같은 마이크로 전자 산업의 급속한 발전 MEMS(Micro-Electromechanical Systems), 마이크로 센서, 지능형 카드 및 이식형 마이크로 의료기기, 통합 수요 증가로 이어져 초소형 에너지 저장장치[1,2]. 사용 가능한 배터리 기술 중, 전고체박막리튬전지(TFLB)가 이상적인 대안으로 꼽힌다. 높은 안전성, 작은 크기, Power-on-Chip 설계, 긴 사이클 수명 및 낮은 자체 방전율. 중 하나로서 TFLB의 핵심 부품인 고체박막전해질은 TFLB의 특성을 결정하는 역할[3]. 그러므로, 고성능 고체박막 전해질 개발은 언제나 TFLB 개발의 중요한 목표입니다. 현재 가장 널리 사용되는 TFLB의 전해질은 비정질 리튬인산질화물(LiPON)입니다. 중간 정도의 이온 전도도(2Ã10-6 S...cm-1), 낮은 전자 전도도(~10-14 S...cm-1), 넓은 전압 창(~5.5V), 리튬[4,5]과의 접촉 안정성이 우수합니다. 그러나 그 이온 전도도가 상대적으로 낮아 향후 개발을 방해합니다. 다가오는 사물인터넷(IoT) 시대를 위한 고전력 TFLB[6]. 따라서, 이온 전도도를 높인 새로운 박막 전해질 개발이 시급하며, 큰 전압 범위와 리튬과의 우수한 접촉 안정성 차세대 TFLB.
다양한 무기 고체 전해질 소재 중 Li2O-SiO2 고체 용액 시스템과 그 중수소 생성 단계는 잠재적으로 얇은 것으로 확인되었습니다 빠른 3차원 리튬 전도로 인한 필름 전해질 채널[7]. 예를 들어 Chen 외.[8] 보고됨 Al 치환된 Li4.4Al0.4Si0.6O4-0.3Li2O 고체 전해질은 5.4Ã10-3 Sâcm-1 at 200 â. Adnan 외.[9] Li4Sn0.02Si0.98O4 화합물 발견 주변 온도에서 최대 전도도 값은 3.07×10-5 S×cm-1입니다. 하지만, Li2O-SiO2 전해질 시스템에 대한 이전 연구는 주로 분말에 초점을 맞췄습니다. 결정성이 높은 물질에 대한 연구는 매우 제한적이었지만 TFLB에 대한 비정질 박막 대응물. TFLB는 일반적으로 양극, 전해질, 양극층을 박막으로 증착하여 제작 층, 전해질 필름은 상대적으로 낮은 온도에서 준비되어야합니다 음극과 전해질 사이의 불리한 상호 작용을 피하기 위해, 이는 TFLB[1,2]의 균열 및 단락을 초래합니다. 따라서, 낮은 온도에서 제조된 비정질 특성을 갖는 Li2O-SiO2 전해질 개발 TFLB에는 온도가 중요합니다. 최근 작품[6]이 표시되지만 비정질 Li-Si-P-O-N에 의해 2.06×10-5 S×cm-1의 높은 리튬 이온 전도도를 얻을 수 있음 박막, 전극과의 접촉 안정성 및 전기화학 TFLB의 안정성은 아직 조사되지 않았습니다. 그러므로 비판적으로 고성능 Li2O-SiO2 기반 박막 전해질 개발이 중요 TFLB에서 실제 적용을 시연합니다.
본 연구에서는 비정질 리튬실리콘산질화물(LiSiON) 박막을 사용하였다. 실온에서 무선 주파수(RF) 마그네트론 스퍼터링으로 제조되었으며, TFLB의 고체 전해질로 연구되었습니다. 스퍼터링 파워와 최적의 증착 조건을 얻기 위해 N2/Ar 작업 가스의 흐름을 최적화했습니다. LiSiON박막용. 또한, 적용 가능성을 입증하기 위해 TFLB에 최적화된 LiSiON 전해질, MoO3/LiSiON/Li 풀셀을 구축하고 전기화학적 성능을 체계적으로 조사하였다.
1 실험
1.1 LiSiON 박막의 제조
LiSiON 박막은 RF 마그네트론 스퍼터링으로 제조되었습니다(Kurt J. Lesker)는 실온에서 Li2SiO3 타겟(직경 76.2mm)을 사용하여 12시 증착 전에 챔버의 압력은 다음보다 낮은 수준으로 감소되었습니다. 1×10-5 Pa. 타겟에서 기판까지의 거리는 10cm였습니다. 샘플 90sccm N2 흐름에서 80, 100, 120W의 RF 전력으로 증착된 것은 각각 샘플 LiSiON-80N9, LiSiON-100N9 및 LiSiON-120N9로 표시되어 있습니다. 그리고 90sccm N2 및 10의 흐름에서 100W의 RF 전력으로 증착된 샘플 sccm Ar, 90 sccm N2 및 50 sccm Ar, 50 sccm N2 및 50 sccm Ar은 샘플 LiSiON-100N9A1, LiSiON-100N9A5로 표시되어 있으며 LiSiON-100N5A5
MoO3 필름은 직류(DC) 반응성 마그네트론으로 제조되었습니다. 순금속 Mo 타겟(직경 76.2mm)을 이용한 스퍼터링(Kurt J. Lesker) 이전 보고서에 따르면[10]. 타겟에서 기판까지의 거리는 10cm이고, DC 스퍼터링 전력은 60W였습니다. 증착은 기판에서 수행되었습니다. 40sccm Ar 및 10sccm의 흐름에서 4시간 동안 100°C의 온도 O2, 이어서 450°C에서 1시간 동안 현장 어닐링 처리. LiSiON-100N9A1은 MoO3 필름 위에 다음과 같이 증착되었습니다. 전해질. 그 후 약 2μm 두께의 금속 리튬막을 제작하였다. 진공 열 증발에 의해 LiSiON 필름 위에 증착되었습니다(Kurt J. Lesker). 최종 제조 단계에는 Cu 집전체의 증착과 캡슐화 과정.
결정 구조 샘플을 X선 회절(XRD, Bruker D8 Advance)로 특성화했습니다. 샘플의 형태와 미세구조는 현장별로 특성화되었습니다. 방출주사전자현미경(FESEM, FEI Quanta 250F) 장착 에너지 분산형 X선 분광법(EDS). 의 원소 조성은 샘플은 유도 결합 플라즈마 질량 분석기(ICP-MS, 애질런트 7700X). 샘플의 화학적 조성 및 결합 정보 X선 광전자 분광법(XPS, Escalab 250XI, Thermo)으로 측정하였다. 과학).
1.4 전기화학적 측정
LiSiON 박막 전해질의 이온 전도도를 측정했습니다. Pt/LiSiON/Pt의 샌드위치 구조를 사용합니다. 전기화학적 임피던스 분광학(EIS)(1000kHz ~ 0.1Hz, 잠재적 진폭 5mV) 샘플의 순환 전압전류법(CV) 측정이 생물학적 VMP3 전기화학 워크스테이션. 정전류 충전/방전(GCD) MoO3/LiSiON/Li TFLB 측정은 Neware BTS4000을 사용하여 수행되었습니다. 실온에서 아르곤으로 채워진 글러브 박스에 배터리 시스템이 들어 있습니다. 사르토리우스 분석 저울(CPA225D, 분해능 10μg)을 사용하여 다음을 결정했습니다. 전극 질량 로딩과 MoO3 필름의 질량 로딩은 다음과 같습니다. 약 0.4mg~cm-2.
2 결과 및 논의
그림 1(a)에 삽입된 광학 이미지에서 볼 수 있듯이, LiSiON 박막을 제조하기 위해 Li2SiO3 타겟을 사용했습니다. XRD 결과 그림 1(a)에서 타겟이 주요 Li2SiO3(JCPDS)로 구성되어 있음을 나타냅니다. 83-1517) 상 및 부 SiO2 상. ICP-MS 측정은 원자가 Li:Si의 비율은 목표에서 약 1.79:1이다. 투명한 무정형 얇은 스퍼터링 후 전형적인 샘플 LiSiON-100N9A1에 대해 필름을 얻었습니다. 목표(그림 1(b)). 전형적인 샘플 LiSiON-100N9A1의 두께는 그림 1(c)의 단면 FESEM 이미지는 다음과 같습니다. 약 1.2μm, 약 100nm·h-1의 성장률을 나타냅니다. 이 조건. 그림 1(d)의 평면도 FESEM 이미지에 표시된 것처럼 LiSiON 박막의 표면은 균열이나 균열 없이 매우 매끄럽고 치밀합니다. 핀홀을 만들어 지름길을 방지하고 TFLB에 적합한 고체 전해질로 만듭니다. 안전 문제.
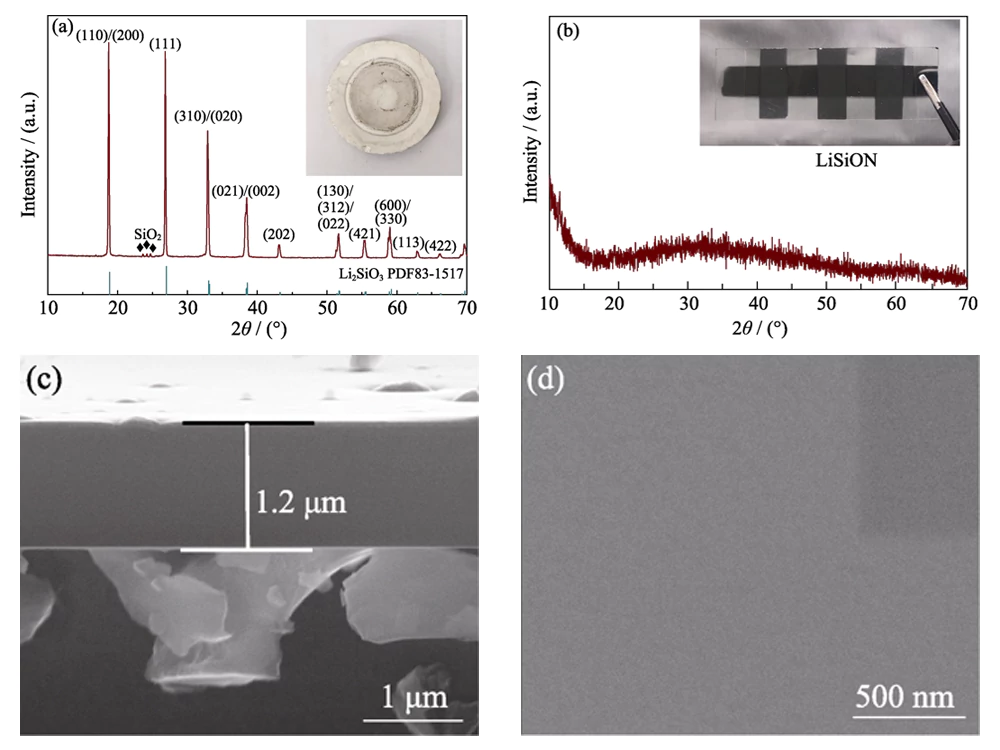
그림 1 (a) Li2SiO3 타겟의 XRD 패턴 및 광학 이미지; (b) XRD 패턴 및 광학 이미지 전형적인 샘플 LiSiON-100N9A1; (c) 단면 및 (d) 평면도 FESEM 이미지 전형적인 샘플 LiSiON-100N9A1
XPS 분석은 화학적 조성을 조사하기 위해 수행되었으며 Li2SiO3 타겟과 일반 샘플 LiSiON-100N9A1의 결합 정보. XPS 설문조사 그림 2(a)의 스펙트럼 스캔 Li2SiO3 타겟에 Li, Si, O 원소가 존재함을 나타냅니다. 그리고 LiSiON 박막에 N 원소를 도입하는 것입니다. 원자 비율 XPS 결과에 따르면 LiSiON 박막의 N:Si는 약 0.33:1이다. ICP-MS에서 얻은 해당 원자비(1.51:1)와 결합 측정에서 일반적인 샘플 LiSiON-100N9A1의 화학양론은 다음과 같습니다. Li1.51SiO2.26N0.33인 것으로 결정되었다. 단일 Si-Si(103.2eV) 피크와 비교하면 Li2SiO3 타겟의 Si2p 코어 레벨 XPS 스펙트럼(그림 2(b)), LiSiON 박막에서 추가적인 Si-N(101.6eV) 피크를 관찰할 수 있으며, 이는 LiSiON[11,12]에서 질화가 발생함을 시사합니다. O1 그림 2(c)의 Li2SiO3 타겟의 코어 레벨 XPS 스펙트럼 두 가지 결합 환경, 즉 SiOx에서 유래한 531.5eV와 528.8eV를 보여줍니다. Li2O에 할당된 eV. 증착 후 530.2에서 추가 구성 요소가 나타났습니다. eV는 LiSiON 박막으로 관찰할 수 있으며, 이는 Non-bridging에 할당될 수 있습니다. 규산염의 산소(On)[13,14]. LiSiON 박막의 N1s 코어 레벨 XPS 스펙트럼 그림 2(d)에서 Si-N 결합의 경우 398.2eV, 396.4eV를 포함하여 3개의 피크로 분리됩니다. Li3N의 경우, 아질산염 종 NO2-의 경우 403.8eV로 N이 LiSiON 네트워크[14,15,16]. 그림 2(e)에 개략적으로 설명된 것처럼, N을 LiSiON 네트워크에 통합하면 더 많은 가교를 형성할 수 있습니다. 빠른 리튬 이온 전도에 유리한 구조[6,17].
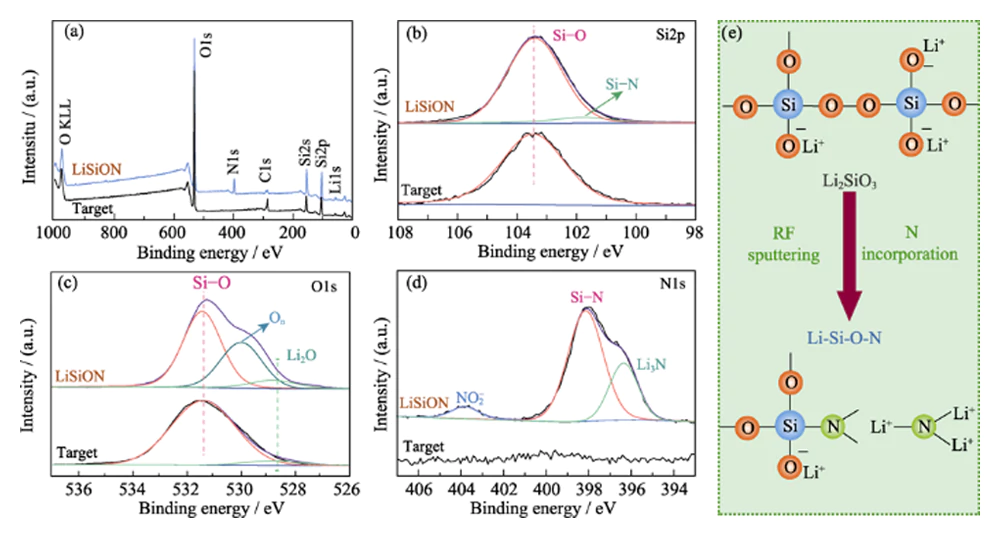
그림. 2 (a) 설문조사 스캔, (b) Si2p 코어 수준, (c) O1s 코어 수준, (d) Li2SiO3 타겟과 일반적인 샘플 LiSiON-100N9A1의 N1s 코어 수준 XPS 스펙트럼; (이자형) N의 통합으로 인해 Li2SiO3에서 LiSiON으로 부분 구조 변화에 대한 개략도
이온 전도도와 전기화학적 안정성을 최적화하기 위해 LiSiON 박막, 서로 다른 스퍼터링으로 증착된 다양한 LiSiON 박막 전력 및 작동 가스 흐름을 이온 측면에서 비교했습니다. 전도도 및 전압 창. 실온의 Nyquist 플롯은 다음과 같습니다. LiSiON 박막은 그림 3(a)에 묘사되어 있습니다. 해당 Pt/LiSiON/Pt 샌드위치 구조 및 등가 회로는 다음과 같습니다. 그림 3(b)에 나와 있습니다. 처럼 관찰한 결과 Nyquist 플롯은 단일 반원과 유전체를 나타냅니다. 박막 전도성 유전체의 특징인 커패시턴스 테일 차단 접점 사이에 벌크 완화 프로세스가 삽입되어 있습니다[17]. 이온 LiSiON 박막의 전도도(Ïi)는 식을 사용하여 계산할 수 있습니다. (1).
Ïi=d/(RA)
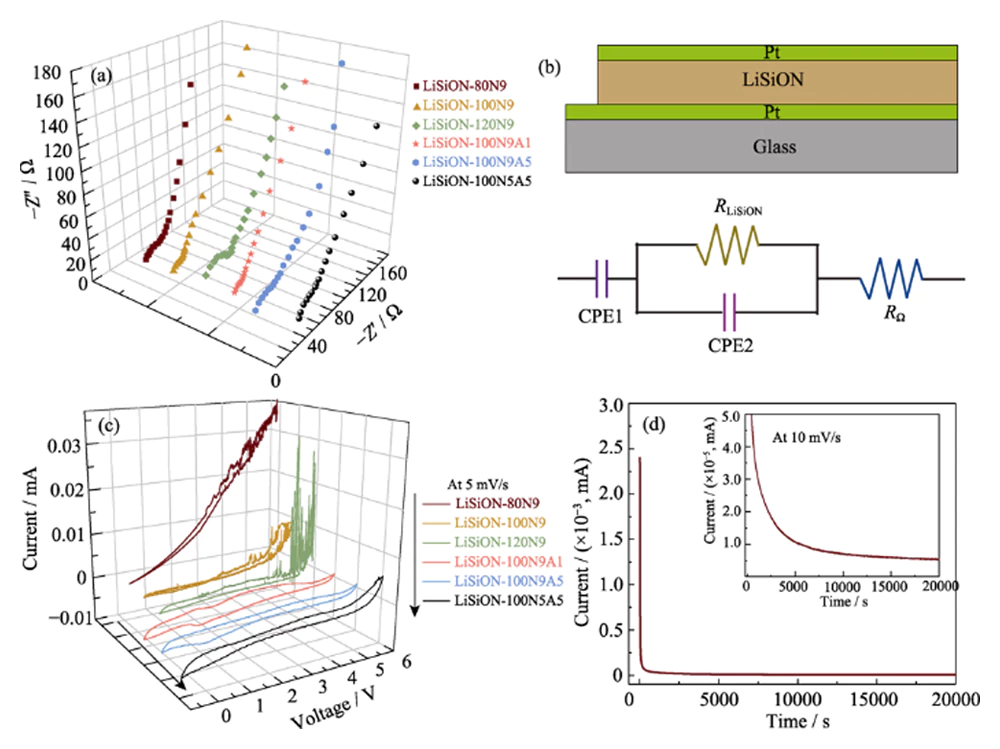
그림. 3 (a) 전기화학적 임피던스 분광법(EIS) 스펙트럼 서로 다른 조건에서 증착된 LiSiON 박막; (b) 개략도 Pt/LiSiON/Pt 샌드위치 구조 및 해당 구조의 그림 등가회로; (c) 증착된 LiSiON 박막의 CV 곡선 다른 조건; (d) 샘플 LiSiON-100N9A1의 대시간 전류측정 곡선
여기서 d는 필름 두께이고, A는 유효 면적(약 1cm2), R은 추정된 필름 저항입니다. 측정된 Nyquist 플롯에서. 이들에 대해 계산된 이온 전도도 LiSiON 박막은 표 1에서 비교됩니다. 관찰된 바와 같이, 증착된 LiSiON 박막의 이온 전도도는 90sccm의 일정한 흐름에서 N2는 80W에서 스퍼터링 전력이 증가함에 따라 증가합니다. 100W로 증가한 다음 스퍼터링 전력이 120W로 더 높아지면 감소합니다. W는 LiPON 전해질에 대한 이전 보고서와 유사합니다[18]. 명백한 이온 전도도의 증가는 N2 비율이 다음과 같을 때 관찰될 수 있습니다. 100W의 일정한 스퍼터링 전력 하에서 작업 가스가 촉진됩니다. 이는 질소 함유량이 증가했기 때문일 수 있습니다. 리튬 이온 이동에 더 유리한 환경을 갖춘 LiSiON[5, 18]. 눈에 띄게, 샘플 LiSiON-100N9 및 LiSiON-100N9A1은 가장 높은 이온성을 나타냅니다. 전도율은 각각 7.1×10-6 및 6.3×10-6 S…cm-1이며 이는 분명히 더 높습니다. 잘 알려진 LiPON(~2×10-6 S×cm-1), 이전에 보고된 비정질 LiNbO3(~1×10-6 S×cm-1)[19], LiBON(2.3×10- 6 S...cm-1)[20], Li-V-Si-O (~1ø10-6 Søcm-1)[21], Li-La-Zr-O (4ø10-7 Søcm-1)[22] 및 Li-Si-P-O (1.6Ã10-6 Sâcm-1)[23] 전해질 필름은 비정질을 나타냅니다. LiSiON 박막은 TFLB용 전해질로서 경쟁력 있는 후보이다. 높은 LiSiON 박막의 이온 전도도는 N을 박막으로 형성하고 Si-O 결합 대신 Si-N 결합을 형성하며, 용이한 리튬 이온에 대한 보다 망상형 음이온 네트워크로 이어짐 이동성[17, 24]. LiSiON의 전기화학적 안정 전압 창 박막은 5mV·s-1의 스캔 속도에서 CV 측정으로 평가되었습니다. 최대 5.5V의 전압. 증착의 영향이 지적되어야 합니다. LiSiON 필름의 전압 창 조건은 다양하므로 현재 관련 연구가 없기 때문에 명확한 메커니즘으로 설명됩니다. 박막 전해질에 관한 이전 보고서[18,24-25]. 그럼에도 불구하고, 그림 3(c)와 비교 표 1에서, 샘플 LiSiON-100N9A1 및 LiSiON-100N5A5는 가장 넓은 전압을 보여줍니다. LiPON에 가까운 각각 ~5.0 및 ~5.2V의 창 전해질. 따라서 이온 전도도와 전압 창을 모두 취했습니다. 이를 고려하여 추가 조사를 위해 샘플 LiSiON-100N9A1이 선택되었습니다. 그리고 풀셀을 제작합니다. 리튬 이온 이동을 탐색하려면 샘플의 수(Ïi) 및 전자 전도도(Ïe) LiSiON-100N9A1, 정전압에서 시간전류 측정을 추가로 수행했습니다. 10mV(그림 3(d)). Ïi는 Eq.로 계산할 수 있습니다. (2).
Ïi=(Ib-Ie)/Ib
여기서 Ib는 초기 분극 전류이고 Ie는 정상 전류입니다. 상태 전류[18]. Ïi는 0.998로 계산되었습니다. 1에 가까우며, 이는 리튬 이온 전도가 절대적으로 지배적임을 나타냅니다. 전해질에서. Ïi는 다음의 혼합 효과에 의해 결정됩니다. 이온과 전자의 전도[24]는 Eq. (3).
Ïi=Ïi/(Ïi+Ïe)
따라서 시료 LiSiON-100N9A1의 Ïe는 다음과 같이 계산됩니다. 1.26ø10-8 Søcm-1이며, 이는 이온 전도성에 비해 무시할 수 있는 수준입니다.
표 1 리튬이온 전도도 및 전압 비교 다양한 조건에서 증착된 LiSiON 박막의 창
|
샘플 |
리튬이온 전도도 |
전압 |
|
LiSiON-80N9 |
4.6 |
~2.0 |
|
LiSiON-100N9 |
7.1 |
~3.9 |
|
LiSiON-120N9 |
2.5 |
~4.2 |
|
LiSiON-100N9A1 |
6.3 |
~5.0 |
|
LiSiON-100N9A5 |
3.0 |
~4.6 |
|
LiSiON-100N5A5 |
2.9 |
~5.2 |
최적화된 샘플 LiSiON-100N9A1의 타당성을 검증하기 위해 TFLB를 적용하여 MoO3/LiSiON/Li TFLB를 추가로 제작하였다. 단면 MoO3/LiSiON/Li TFLB의 FESEM 이미지 및 해당 EDS 매핑 이미지 그림 4(a)에 나와 있습니다. 처럼 관찰된 MoO3 음극(두께 약 1.1μm)과 Li 양극 LiSiON 전해질에 의해 잘 분리되어 있으며 LiSiON 전해질은 음극과 양극 모두와 긴밀한 접촉 인터페이스를 갖습니다. 그림 4(b) 0.1mV…s-1 사이의 스캔 속도로 TFLB의 일반적인 CV 곡선을 표시합니다. 1.5-3.5V, 약 2.25와 2.65에서 잘 정의된 한 쌍의 산화환원 피크를 나타냅니다. V는 MoO3에 리튬 이온 삽입 및 추출에 해당합니다[10]. 그림 4(c) 는 TFLB의 초기 3개 정전류 충전/방전 곡선을 나타냅니다. 전류 밀도는 50mA·g-1(20μA·cm-2, MoO3 필름 질량 기준)입니다. 관찰된 바와 같이 TFLB는 다음을 제공합니다. 초기 충전/방전 용량은 145/297mAh…g-1(58/118.8 ¼아…cm-2). 2번째 사이클 이후에는 높은 가역성을 지닌 꾸준한 사이클링 동작 TFLB는 282mAh...g-1의 특정 용량을 달성했습니다. 속도 성능 다양한 전류 밀도에서의 TFLB는 그림 4(d)에 나와 있습니다. 그만큼 저전류에서 초기 여러 사이클에서 TFLB의 비가역적 용량 손실 밀도는 MoO3에서 파생된 돌이킬 수 없는 상전이로 인해 발생할 수 있습니다. 리튬 삽입에 의한 것[26]. 약 219, 173, 107 등의 안정적인 방전용량 50mAh...g-1은 각각 100, 200, 400, 800mA...g-1에서 관찰됩니다. 좋은 속도 능력을 보여줍니다. 전기화학적 안정성을 평가하려면 TFLB의 사이클 성능은 전류 밀도에서 추가로 수행되었습니다. 200mA...g-1(그림 4(e)). TFLB는 200사이클 후에도 초기 방전 용량의 78.1%를 유지할 수 있으며, 쿨롱 효율은 각 사이클마다 100%에 가까워 허용 가능한 수준을 나타냅니다. LiSiON 전해질의 전기화학적 안정성. EIS 측정값은 다음과 같습니다. 조사하기 위해 개방 회로 전압에서 추가로 수행되었습니다. 서로 다른 사이클 수에서 TFLB의 전해질/전극 인터페이스 등가 회로가 있는 해당 Nyquist 플롯이 그림 4(f)에 표시되어 있습니다. 처럼 관찰된 바에 따르면, MoO3/LiSiON/Li TFLB는 다음으로 구성된 유사한 EIS 스펙트럼을 보여줍니다. 신선한 상태의 고주파수 영역에 있는 두 개의 반원의 이전 연구[10]에서는 MoO3/LiPON/Li TFLB를 나타냈습니다. Li/LiSiON 계면 저항은 LiSiON/MoO3 인터페이스[20]. Nyquist 플롯의 첫 번째 작은 반원은 다음과 같습니다. LiSiON 전해질에서 Li+ 이온의 이온 전도에 기인하는 반면, 두 번째 큰 반원은 전하 이동 과정에 해당합니다. LiSiON/MoO3 인터페이스[27,28]. 첫 번째 작은 반원이 나타나는 경우는 거의 없습니다. 주기 동안의 변화는 상대적으로 양호한 주기 안정성을 나타냅니다. LiSiON 전해질. 그러나 두 번째 반원은 다음과 같이 점차 확대됩니다. 사이클 번호가 발전하여 LiSiON/MoO3 계면이 증가함을 나타냅니다. 사이클링 중 저항이 용량의 주요 원인이 될 수 있습니다. TFLB의 페이딩[29]. 이 작업이 성공적으로 수행되었다는 점은 언급할 가치가 있습니다. LiSiON 전해질을 사용하여 TFLB를 구성하고 우수한 성능을 입증합니다. MoO3 음극 및 리튬 양극 모두와 LiSiON의 계면 접촉 처음으로. 더욱이, 큰 비용량, 좋은 비율 능력, MoO3/LiSiON/Li TFLB의 허용 가능한 사이클 성능은 LiSiON이 박막은 TFLB용 전해질로 잘 응용된다.
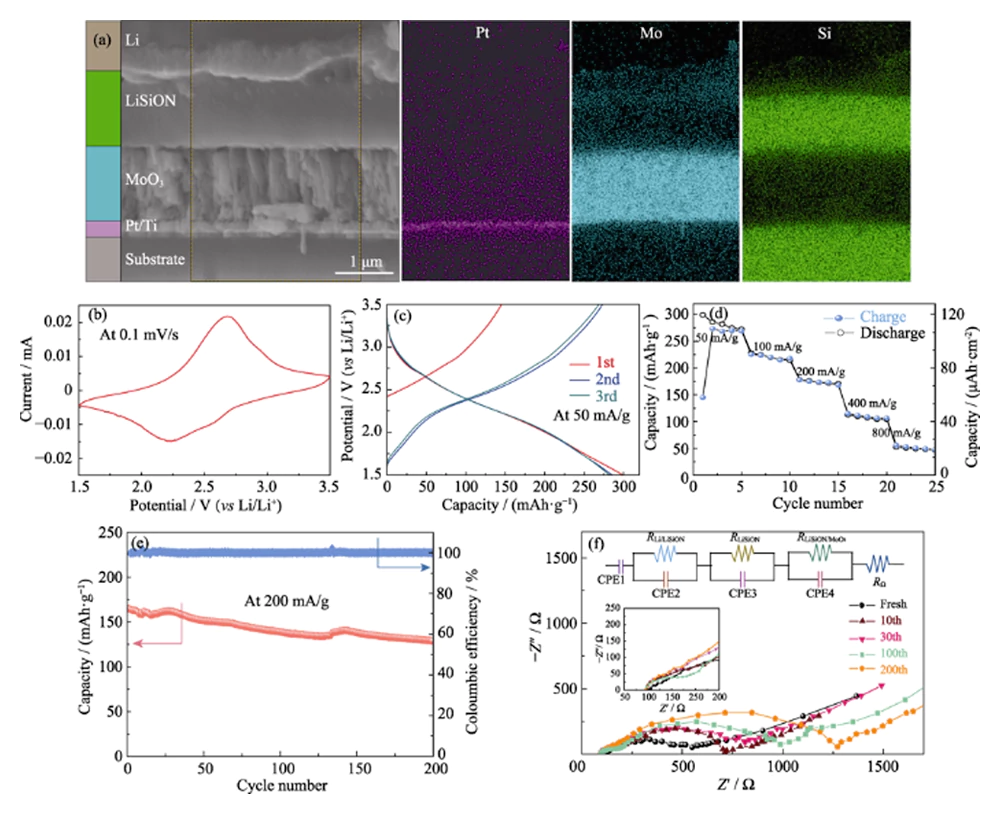
그림. 4 (a) 단면 FESEM 이미지 및 해당 EDS 매핑 MoO3/LiSiON/Li의 이미지 TFLB; (b) 일반적인 CV 곡선, (c) 초기 3개의 충전/방전 곡선, (d) 속도 성능, (e) 사이클 성능, (f) 다른 사이클에서의 EIS 스펙트럼 MoO3/LiSiON/Li의 수 샘플 LiSiON-100N9A1을 전해질로 사용하는 TFLB
3가지 결론
요약하면, 비정질 LiSiON 박막 전해질이 성공적으로 개발되었다. N2/Ar 가스 흐름이 있는 Li2SiO3 타겟을 사용하여 RF 마그네트론 스퍼터링으로 준비되었습니다. 100W의 RF 전력에서 의 흐름으로 증착된 최적화된 LiSiON 박막 90 sccm N2 및 10 sccm Ar은 매끄러운 표면, 조밀한 구조, 높은 이온을 보유합니다. 전도성(6.3×10-6 S…cm-1) 및 넓은 전압 범위(5V)로 인해 유망한 제품입니다. TFLB용 전해질 소재. 더 중요한 것은 LiSiON을 사용함으로써 전해질인 MoO3/LiSiON/Li TFLB가 성공적으로 시연되었습니다. 처음으로 높은 비용량(50mA...g-1에서 282mAh...g-1), 우수한 속도 성능(800에서 50mAh...g-1) mA...g-1) 및 허용 가능한 주기 안정성(200 이후 78.1% 용량 유지) 주기). 이번 작업은 고도의 발전을 위한 새로운 기회를 가져올 것으로 예상됩니다. Li2O-SiO2 기반의 박막전해질을 이용한 TFLB 성능
참고자료
[1] MOITZHEIM S, PUT B, VEREECKEN P M. 3D 박막 리튬 이온 배터리 분야의 발전. 고급 재료 인터페이스, 2019,6(15):1900805.
[2] XIA Q, ZHANG Q, SUN S, 외. 고성능 전고체 박막 리튬 마이크로배터리를 위한 3D 음극으로 터널 내부 성장 LixMnO2 나노시트 어레이. 첨단재료, 2021,33(5):2003524.
[3] DENG Y, EAMES C, FLEUTOT B, et al. 혼합 다중음이온 효과를 통해 리튬 초이온 전도체(LISICON) 고체 전해질의 리튬 이온 전도도를 향상시킵니다. ACS 응용 재료 및 인터페이스, 2017,9(8):7050-7058.
[4] BATES JB, DUDNEY NJ, GRUZALSKI GR, et al. 비정질 리튬 전해질 박막 및 이차박막 전지의 제조 및 특성 규명. 전원 저널, 1993,43(1/2/3):103-110.
[5] BATES J. 비정질 리튬 전해질 박막의 전기적 특성. 솔리드 스테이트 아이오닉스(Solid State Ionics), 1992,53(56):647-654.
[6] FAMPRIKIS T, GALIPAUD J, CLEMENS O, et al. 전고체 배터리용 LiSiPO(N) 박막 전해질의 이온 전도도의 조성 의존성. ACS 응용 에너지 재료, 2019,2(7):4782-4791.
[7] DENG Y, EAMES C, CHOTARD J N, 외. Li4SiO4-Li3PO4 고체 전해질의 빠른 리튬 이온 전도에 대한 구조적 및 기계적 통찰력. 미국화학회지, 2015,137(28):9136-9145.
[8] CHEN R, SONG X. Li4+xMxSi1-xO4-yLi2O(M=Al, B) 시스템에 대한 고체 전해질의 이온 전도도. 중국화학회지, 2002,49:7-10.
[9] ADNAN S, MOHAMED NS. Sn 치환이 Li4SiO4 세라믹 전해질 특성에 미치는 영향. 솔리드 스테이트 이온스(Solid State Ionics), 2014,262:559-562.
[10] SUN S, XIA Q, LIU J, et al. 고급 전고체 박막 리튬 배터리용 3D 음극으로 사용되는 자립형 산소 결핍 α-MoO3-x 나노플레이크 어레이. 재료공학 저널, 2019,5(2):229-236.
[11] DING W, LU W, DENG X, et al. 마이크로파 ECR 마그네트론 스퍼터링으로 증착된 SiNx 필름의 구조에 대한 XPS 연구. Acta Physica Sinica, 2009,58(6):4109-4116.
[12] KIM H, KIM Y. Li4SiO4의 부분 질화 및 Li4의 이온 전도도. 1SiO3. 9N0. 1도자기국제, 2018,44(8):9058-9062.
[13] MARIKO M, HIDEMASA K, TOMOYUKI O, 외. 리튬이온 배터리용 SiO2 양극 분석. 전기화학학회지, 2005,152(10):A2089.
[14] FINGERLE M, BUCHHEIT R, SICOLO S, et al. LiCoO2-LiPON 인터페이스에서의 반응 및 공간 전하층 형성: 결합된 표면 과학 시뮬레이션 접근법을 통한 결함 형성 및 이온 에너지 수준 정렬에 대한 통찰력. 화학재료, 2017,29(18):7675-7685.
[15] WEST W, HOOD Z, ADHIKARI S, et al. 결정질 Li2PO2N 소스로부터 필름을 펄스 레이저 증착하여 고체 전해질-전극 경계면에서 전하 이동 저항을 감소시킵니다. 전원 저널, 2016,312:116-122.
[16] SICOLO S, FINGERLE M, HAUSBRAND R, et al. 리튬에 대한 비정질 LiPON의 계면 불안정성: 밀도 함수 이론과 분광학 연구의 결합. 전원 저널, 2017,354:124-133.
[17] WU F, LIU Y, CHEN R, et al. 리튬박막전지용 신규 Li-Ti-Si-P-O-N 박막전해질 제조 및 성능. 전원 저널, 2009,189(1):467-470.
[18] PUT B, VEREECKEN M, MEERSSCHAUT J, 외. 나노규모 배터리용 초박형 RF 스퍼터링 LiPON 층의 전기적 특성. ACS 응용 재료 및 인터페이스, 2016,8(11):7060-7069.
[19] NIINOMI H, MOTOYAMA M, IRIYAMA Y. Li+ Sol-Gel 방법으로 증착된 Li-Nb-O 막의 전도. 솔리드 스테이트 아이오닉스, 2016,285:13-18.
[20] SONG S, LEE K, PARK H. 리튬붕소산질화물 고체 전해질을 기반으로 한 고성능 유연성 전고체 마이크로배터리. 전원 저널, 2016,328:311-317.
[21] OHTSUKA H, OKADA S, YAMAKI J. Li2O-V2O5-SiO2 고체전해질박막을 이용한 고체전지. 고체 이온공학, 1990,40-41:964-966.
[22] Kalita D, Lee S, Lee K, et al. 박막전지용 비정질 Li-La-Zr-O 고체전해질의 이온전도도 특성. 솔리드 스테이트 아이오닉스, 2012,229:14-19.
[23] SAKURAI Y, SAKUDA A, HAYASHI A, et al. 펄스레이저증착법을 이용한 전고체 리튬이차전지용 비정질 Li4SiO4-Li3PO4박막 제조. 솔리드 스테이트 이온스(Solid State Ionics), 2011,182:59-63.
[24] TAN G, WU F, LI L, 외. 전고체 리튬이온전지용 질소함유 리튬-알루미늄-인산티타늄계 박막전해질의 마그네트론 스퍼터링 제조. 물리화학 저널 C, 2012,116(5):3817-3826.
[25] YU X, BATES JB, JELLISON G, et al. 안정적인 박막 리튬 전해질: 리튬인산질화물. 전기화학학회지, 1997,144(2):524.
[26] KIM H, COOK J, LIN H, et al. 산소 결손은 MoO3-x의 유사 용량성 전하 저장 특성을 향상시킵니다. 자연재료, 2017,16:454-460.
[27] SONG H, WANG S, SONG X 등. 극저온에서 작동하는 태양광 구동 전고체 리튬공기 배터리. 에너지환경과학, 2020,13(4):1205-1211.
[28] WANG Z, LEE J, XIN H, et al. 전고체 박막 배터리의 장기 사이클링에 대한 음극 전해질 계면(CEI) 층의 영향. 전원 저널, 2016,324:342-348.
[29] QIAO Y, DENG H, HE P, et al. 음이온 산화환원을 기반으로 한 500Wh/kg 리튬 금속 전지. 줄, 2020,4(6):1311-1323.



