리튬황 전지용 붕소계 소재의 최근 동향
최근 진행상황 리튬황전지의 붕소계 소재
저자: LI Gaoran, LI 홍양, ZENG Haibo
MIIT 핵심 연구소 첨단디스플레이재료 및 소자, 나노광전자공학연구소 난징대학교 재료공학부 재료 과학기술, 난징 210094
초록
리튬황(Li-S) 배터리 재생 차세대 전기화학에너지 개발의 핵심 역할 에너지 밀도가 높고 비용이 저렴하기 때문에 저장 기술을 사용합니다. 그러나 그들의 실제 적용은 여전히 느린 속도와 낮은 속도로 인해 방해를 받습니다. 상대적으로 낮은 기여를 하는 전환 반응의 가역성 실제 용량, 쿨롱 비효율성 및 사이클링 불안정성. 이에 전도성, 흡착성, 촉매성 기능을 합리적으로 설계 재료는 황을 안정화하고 촉진하는 중요한 경로를 제시합니다. 전기화학. 독특한 원자 및 전자 구조의 이점 붕소계 재료는 다양하고 조정 가능한 물리적, 화학적, 전기화학적 특성을 갖고 있으며 광범위한 연구를 받아왔습니다. Li-S 배터리에 주목하세요. 이 논문에서는 최근 연구 진행 상황을 검토합니다. 보로펜, 보론 원자 도핑 탄소, 금속 등 보론 기반 소재 Li-S 배터리의 붕화물 및 비금속 붕화물, 나머지 결론 문제를 해결하고 향후 발전 방향을 제시합니다.
키워드:리튬황 배터리, 붕화물, 화학적 도핑, 보로펜, 셔틀 효과, 리뷰
녹색 신재생에너지를 개발하고, 첨단 에너지 전환 및 저장 방법을 개발하고, 효율적이고 깨끗한 에너지 시스템은 환경 문제를 해결하기 위한 불가피한 선택입니다. 오늘날 세계의 에너지 위기와 기후 변화. 전기화학적 에너지 배터리로 대표되는 저장 기술을 통해 깨끗한 새 제품으로 변환하여 저장할 수 있습니다. 에너지를 보다 효율적이고 편리한 형태로 활용하여 녹색 에너지 경제와 지속 가능한 발전을 촉진하는 데 중요한 역할 [1,2]. 많은 배터리 기술 중에서 리튬이온 배터리는 에너지 밀도가 높고 메모리 효과가 없다는 장점이 있습니다. 급속한 성과를 거두었습니다 1991년 상용화 이후 개발되었으며, 전기 자동차, 휴대용 전자 장치, 국방 및 기타 필드 [3,4]. 그러나 지속적인 전기기기의 발전으로 인해 전통적인 리튬이온 배터리는 증가하는 에너지를 감당할 수 없었습니다. 수요. 이러한 배경에서 리튬-황 배터리가 널리 주목을 받고 있습니다. 높은 이론적 비용량(1675 mAh·g-1)으로 인해 주목을 받고 있으며, 에너지 밀도(2600Wh·kg-1). 동시에, 유황 자원은 풍부하고, 널리 분포되어 있으며, 가격이 저렴하고, 환경 친화적인 리튬-황 배터리를 연구 핫스팟으로 만들고 있습니다. 최근 신규 이차전지 분야[5,6].
1 작동 원리와 기존 문제점 리튬황전지
리튬-황 배터리는 일반적으로 사용됩니다. 양극은 황 원소, 음극은 금속 리튬 전극. 기본 배터리 구조는 그림 1(a)에 나와 있습니다. 그만큼 전기화학 반응은 다음과 같은 다단계 전환 반응 과정이다. 고체-액체 상전이를 수반하는 다중 전자 이동 및 일련의 리튬 폴리설파이드 중간체(그림 1(b)) [7,8]. 그 중, 원소 황과 단쇄 Li2S2/Li2S는 양쪽 끝에 위치 반응 사슬은 전해질에 불용성이며 다음과 같은 형태로 존재합니다. 전극 표면에 침전이 발생합니다. 장쇄 리튬폴리설파이드(Li2Sx, 4...x...8)은 전해질에서 더 높은 용해도와 이동 능력을 가지고 있습니다. 기반 전극 재료의 고유 특성과 고액상 변환 반응 메커니즘, 리튬-황 배터리는 에너지와 비용상의 이점이 있지만 많은 문제와 과제에 직면해 있습니다 [9,10,11,12]:
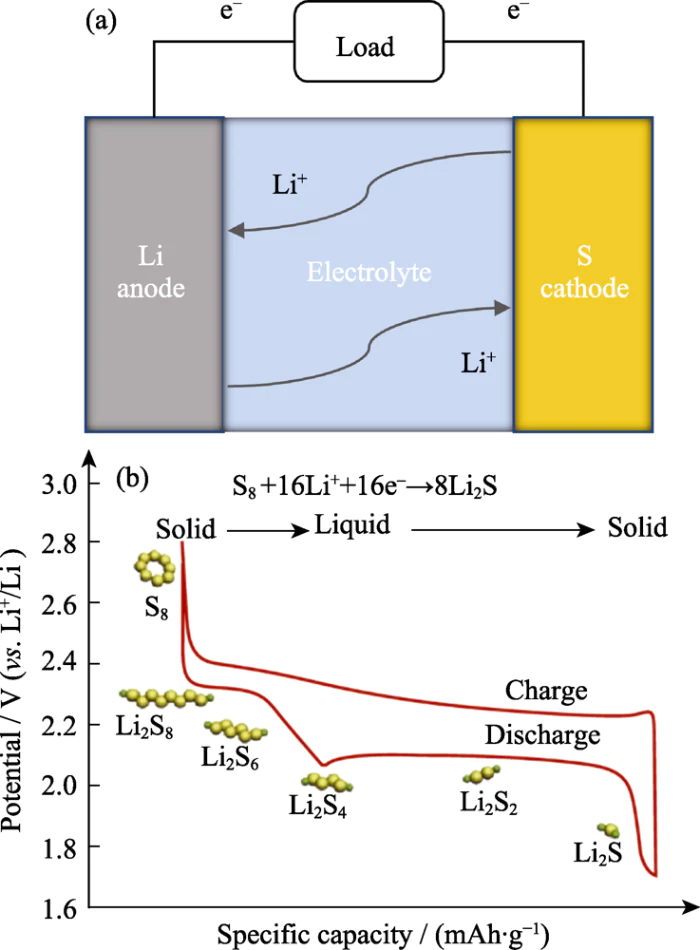
그림. 1 (a) 리튬-황 배터리의 개략도 구성 및 (b) 해당 충방전 과정[7]
1) 고상 원소 황 및 Li2S 전극 표면에 축적되고, 그 고유의 전자와 이온 관성으로 인해 전하 전달이 어려워지고 반응 속도가 느려집니다. 이로 인해 활물질의 활용률이 감소하고 실제 배터리 용량.
2) 밀도차이가 크다 반응 사슬의 양쪽 끝에서 황과 Li2S 사이(2.07 대 1.66 g·cm-3). 재료는 도중에 최대 80%의 부피 변화를 경험합니다. 반응과정, 전극의 기계적 구조적 안정성 엄청난 도전에 직면해 있습니다.
3) 용해 및 이동 거동 전해질 내 폴리황화리튬은 심각한 "셔틀"을 유발합니다. 효과"로 인해 심각한 활물질 손실과 쿨롱 손실이 발생합니다. 또한 리튬폴리설파이드는 화학/전기화학적 측면에도 참여하고 있습니다. 양극 표면에서의 반응으로 인해 활성 물질의 추가 손실이 발생할 뿐만 아니라 재료뿐만 아니라 양극 표면을 부동태화하고 부식시켜 리튬 수지상 결정의 형성 및 성장을 촉진하고 안전 위험을 증가시킵니다.
이러한 문제는 상호 연관되어 있으며 서로 영향을 미치므로 배터리의 복잡성이 크게 증가합니다. 현재의 리튬-황 배터리는 이러한 요구 사항을 충족하기 어렵습니다. 활물질 활용 측면에서 실용화 필요성, 실제 에너지 밀도, 사이클 안정성 및 안전성. 위의 분석을 통해 문제를 해결하면 황 전기화학적 공정을 합리적으로 제어할 수 있음을 알 수 있습니다. 반응 과정은 리튬-황의 성능을 향상시키는 유일한 방법입니다 배터리. 효과적인 유황 관리 및 개선 방법 전기화학은 목표 설계, 개발 및 적용에 따라 달라집니다. 첨단 기능성 소재. 그 중 가장 대표적인 전략은 전도성, 흡착성, 촉매성을 갖는 기능성 소재 개발 황 음극 호스트 또는 수정된 분리막과 같은 특성. 그 물리적인 방법을 통해 리튬폴리설파이드와의 화학적 상호작용을 통해 활성물질은 양극 부위에 국한되어 용해와 확산을 억제하고, 그리고 전기화학적 전환을 촉진합니다. 이로써 셔틀을 완화 효과 및 배터리의 에너지 효율 및 사이클 안정성 향상 [13,14]. 이러한 아이디어를 바탕으로 연구자들은 다양한 유형의 탄소 소재를 포함한 기능성 소재를 타겟 방식으로 전도성 고분자, 금속 유기 골격, 금속 산화물/황화물/질화물, 등 좋은 결과를 얻었습니다 [15,16,17,18,19].
2 붕소계 물질의 응용 리튬-황 배터리
붕소는 가장 작은 준금속 원소입니다. 원자 반경이 작고 전기 음성도가 커서 형성이 쉽습니다. 금속 공유 화합물. 붕소 원자는 전형적인 전자 결핍을 가지고 있습니다. 구조이며 원자가 전자 구성은 2s22p1입니다. 그들은 공유할 수 있습니다 다양한 혼성화 형태를 통해 하나 이상의 전자를 다른 원자와 결합시켜 다중 중심 결합을 형성합니다 [20,21]. 이러한 특성은 붕소를 만듭니다. 고도로 조정 가능한 구조로 독특하고 풍부한 화학적, 물리적 특성을 보여줍니다. 재산은 경공업과 같은 많은 분야에서 널리 이용될 수 있습니다 건축자재, 국방, 에너지 등 [22,23]. 이에 비해, 리튬-황 배터리의 붕소 기반 소재에 대한 연구는 아직 단계적입니다. 초기. 최근에는 나노기술과 특성화 방법이 계속해서 발전하고 있으며, 붕소계의 구조적 특성은 소재는 지속적으로 연구, 개발되어 목표를 달성하고 있습니다. 리튬-황 시스템에 대한 연구 및 응용도 나타나기 시작했습니다. ~ 안에 이러한 관점에서 본 기사에서는 다음과 같은 일반적인 붕소 기반 재료에 중점을 둡니다. 보로펜, 붕소 원자 도핑 탄소, 금속 붕화물, 비금속 붕화물. 이것 기사에서는 리튬-황 배터리의 최신 연구 진행 상황을 검토하고, 기존 문제를 요약하고 향후 개발을 기대합니다. 방향.
2.1 보렌
가장 대표적인 동소체로서 붕소 원소, 보로펜은 단일 원자 두께의 2차원 구조를 가지고 있습니다. 그래핀과 비슷하다. 벌크형 붕소원소와 비교하여 우수한 특성을 나타냄 전기적, 기계적, 열적 특성을 지닌 떠오르는 스타입니다. 2차원 재료[24]. 토폴로지 차이를 기반으로 붕소 원자의 배열, 보로펜은 풍부한 결정 구조를 가지고 있으며 전자 특성뿐만 아니라 이방성 전도성 특성도 포함됩니다. 가능한 한 그림 2(a, b)에서 볼 수 있듯이 보로펜의 전자는 붕소 원자의 꼭대기에 위치하며 이러한 전자 분극 영역은 결합력이 더 높습니다. 활동. 좋은 화학 흡착 장소를 제공할 것으로 기대됩니다. 리튬-황 배터리 시스템의 다황화물[25] 동시에, 보로펜 필름은 전기 전도성이 좋고 물리적, 화학적으로 우수합니다. 안정성이 높아 리튬-황 전지에 응용 가능성이 좋다.
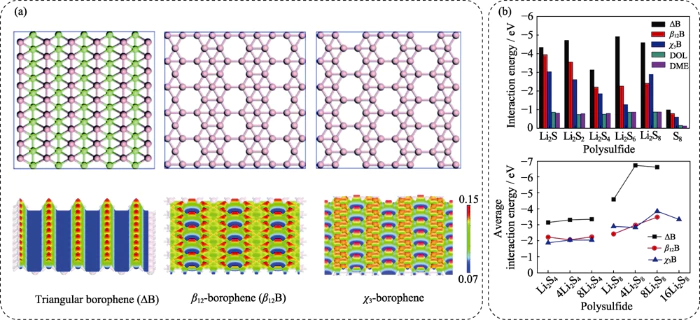
그림 2 (a) 다양한 보로펜의 구조 모델과 해당 전하 밀도 분포, (b) 흡착 에너지 다양한 보로펜의 다황화물[25]
Jianget al. [26] 이론적으로 발견 보로펜은 리튬에 대한 강력한 흡착 능력을 나타내는 것으로 계산됩니다. 다황화물. 그러나 이러한 강력한 상호작용은 또한 다음과 같은 문제를 쉽게 유발할 수도 있습니다. Li-S 클러스터가 분해되어 활성 물질인 황이 손실됩니다. 재료. 이에 비해 본질적인 결함이 있는 보로펜의 표면은 구조는 리튬 폴리설파이드를 보다 부드럽게 흡착하여[27] 분해 및 파괴를 피하면서 셔틀 동작을 제한합니다. 고리 구조. 보다 적합한 리튬이 될 것으로 예상됩니다. 다황화물 흡착 재료. 동시에 에너지 밴드 분석 보로펜-리튬 폴리설파이드 흡착 구조의 결과는 흡착 클러스터는 금속성이며, 이는 주로 본질적인 금속성으로 인해 발생합니다. 붕소의 특성과 강한 전기음향 결합 강도. 그것 황의 전기화학적 전환과정에 도움을 줄 것으로 기대된다. 더 나은 반응 역학 [28]. 또한, Grixti et al. [29] 시뮬레이션 리튬 폴리설파이드 분자의 표면 확산 과정 β12-보렌. β12-borene이 계열에 강한 흡착을 보이는 것으로 밝혀졌습니다. 리튬폴리설파이드. Li2S6의 가장 낮은 확산 에너지 장벽 및 안락의자 방향의 Li2S4 분자는 각각 0.99 및 0.61 eV이며, 지그재그 방향으로 확산하는 것보다 쉽습니다. 그 좋은 덕분에 흡착 능력과 적당한 확산 에너지 장벽, β12-borene은 우수한 리튬 폴리설파이드 흡착 재료로 간주됩니다. 리튬-황 배터리의 셔틀 효과를 억제하고 개선할 것으로 기대 황 전기화학 반응의 가역성.
그러나 현재의 대부분의 연구는 리튬-황 배터리의 붕소 희석은 여전히 이론적 예측에 머물러 있습니다. 단계 및 실험적 확인은 거의 보고되지 않습니다. 이는 주로 붕소 희석액을 준비하는 데 어려움이 있습니다. 붕소의 존재는 1990년대에 예측되었으나 실제로는 2015년까지 준비되지 않았다[30]. 부분 그 이유 중 하나는 붕소가 단지 3개의 원자가 전자만을 갖고 있기 때문일 수 있습니다. 누락된 전자를 보상하기 위한 골격 구조를 형성하여 2차원 구조보다는 3차원 구조를 형성하는 것이 더 쉽습니다. 현재 준비작업은 붕소는 일반적으로 분자선 에피택시와 높은 수준의 기술에 의존합니다. 진공, 고온 및 기타 조건이며 합성 임계값은 높다 [31]. 그러므로 보다 간단하고 효율적인 방법을 개발할 필요가 있다. 붕소희석 합성법을 추가로 실험적으로 탐구하고 리튬-황 전지에서 그 효과와 관련 메커니즘을 입증한다.
2.2 붕소 원자가 도핑된 탄소
화학적으로 도핑된 탄소 재료는 뜨겁습니다. 신에너지 연구 분야의 소재. 적절한 원소 도핑 가능 가볍고 높은 탄소 소재의 장점은 그대로 유지 전도성을 부여하는 동시에 추가적인 물리적, 화학적 특성을 부여합니다. 다양한 애플리케이션 시나리오에 적응합니다[32,33]. 화학적으로 도핑된 탄소 재료는 리튬-황 배터리[34,35]에서 널리 연구되어 왔습니다. 질소 원자와 같은 전기 음성도가 높은 원자로 도핑하는 것이 더 좋습니다. 흔한. 대조적으로, 붕소는 전자가 부족한 구조를 갖고 있으며, 탄소보다 전기 음성이다. 결합 후 양극이 됩니다. 탄소 격자에. 좋은 흡착효과를 기대할 수 있습니다. 음으로 하전된 다황화물 음이온으로 인해 셔틀 효과가 완화됩니다. [36,37].
Yanget al. [38] 붕소가 도핑된 다공성을 사용함 탄소를 황 음극 호스트 물질로 사용하여 붕소 도핑뿐만 아니라 탄소재료의 전자전도도를 향상시켰을 뿐만 아니라 탄소 매트릭스의 양극화. 음으로 하전된 다황화물 이온 정전기 흡착을 통해 효과적으로 흡착 및 고정되며, 루이스 상호작용으로 인해 용해 및 확산이 억제됩니다(그림 3(a, b)). 따라서 붕소가 도핑된 다공성탄소를 기반으로 한 황 음극은 순수 카본보다 더 높은 초기 용량과 더 안정적인 사이클링 성능 그리고 질소가 첨가된 샘플. Xu et al. [39] 붕소 원자가 도핑된 탄소 획득 수열을 통한 나노튜브/황 복합 양극재(BUCNTs/S) 원팟 방식. 액상 현장 합성으로 황을 더욱 균일하게 만듭니다. 복합재에 분포되고 붕소 도핑은 탄소 기반 호스트를 제공합니다. 재료의 전기 전도성이 높고 유황 고정 능력이 더 강합니다. 그만큼 그 결과 BUCNTs/S 전극은 0.2C에서 1251mAh·g-1의 초기 용량을 얻었고 400사이클 후에도 여전히 750mAh·g-1의 용량을 유지할 수 있었습니다. 황 음극 호스트 외에도, 붕소가 첨가된 탄소 재료는 또한 디자인에 중요한 역할을 합니다. 배터리 기능 분리기. Hanet al. [40] 코팅된 경량 붕소 도핑 기능적 변형을 구성하기 위한 전통적인 분리기의 그래핀 효과적으로 완화하기 위해 폴리설파이드의 흡착 및 재사용을 사용하는 층 셔틀효과를 높여 활물질의 이용률을 향상시킨다.
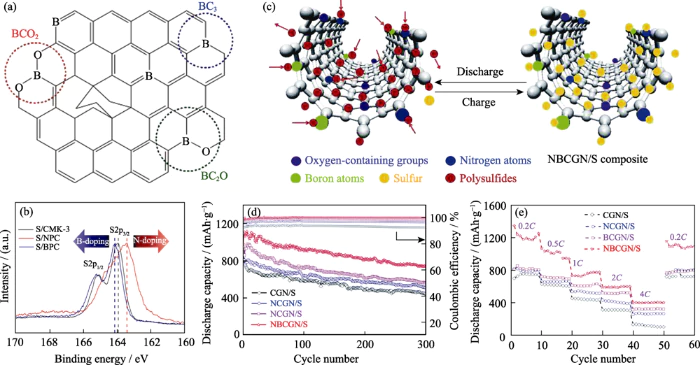
그림. 3 (a) B 도핑 탄소 백본 구성, (b) S2p XPS 다양한 원소가 도핑된 다공성 탄소를 기반으로 한 황 복합재의 스펙트럼; (c) NBCGN/S 복합재의 충방전 과정 계획, (d) 사이클링 0.2C 및 (e) 다음을 기반으로 한 황 전극의 속도 성능 다른 원소가 도핑된 곡선형 그래핀 나노리본[44]
의 기본 특성을 고려하여 다양한 도핑 원소와 탄소에서의 다양한 작용 모드 격자 구조, 다중 원소 공동 도핑은 중요한 전략 중 하나입니다. 탄소재료의 표면화학 조절 및 황 개선 전기화학 반응[41, 42, 43]. 이에 대해 Kuang 연구팀은 [44] 합성된 질소 및 붕소 공동 도핑 그래핀 나노리본(NBCGN) 처음으로 수열법을 통해 호스트 물질로 사용 그림 3(c)와 같이 황 음극. 연구 결과 시너지 효과가 있는 것으로 나타났습니다. 질소와 붕소 공동 도핑의 효과는 NBCGN이 더 큰 것을 얻도록 유도할 뿐만 아니라 비표면적, 기공 부피 및 더 높은 전도성을 제공할 뿐만 아니라 음극에 황을 균일하게 분포시킵니다. 더 중요한 것은 붕소와 질소는 공동 도핑된 물질에서 전자가 부족하고 전자가 풍부한 중심으로 작용합니다. 체계. Lewis를 통해 각각 Sx2- 및 Li+와 결합할 수 있습니다. 상호 작용을 통해 폴리황화리튬을 보다 효율적이고 크게 흡착합니다. 배터리의 사이클 및 속도 성능을 향상시킵니다(그림 3(d, e)). 기반을 둔 전기음성도가 높은 원소와 낮은 원소의 유사한 도핑 전략에 대해. 진 등 알. [45] 붕소와 산소가 함께 도핑된 다중벽 탄소나노튜브 호스트 제조 붕산을 도펀트로 사용한 물질. 결과 배터리는 여전히 100사이클 후 비용량은 937mAh·g-1입니다. 일반 탄소 기반 배터리 성능보다 훨씬 우수합니다. 튜브(428mAh…g-1). 또한 연구자들은 다음과 같은 시도도 했습니다. 다른 공동 도핑 형태. 붕규산염 공동 도핑된 그래핀[46], 코발트 포함 금속 및 붕소 질소 공동 도핑된 그래핀[47] 등은 효과적으로 배터리 성능이 향상되었습니다. 공동 도핑된 성분의 시너지 효과 황의 전기화학적 반응을 개선하는데 중요한 역할을 한다.
붕소 원소 도핑을 효과적으로 수행할 수 있습니다. 탄소의 고유 전도성과 표면 화학적 극성을 향상시킵니다. 재료, 화학 흡착을 강화하고 셔틀 동작을 억제합니다. 리튬 폴리설파이드를 사용하여 황 전기화학 반응 역학을 향상시킵니다. 안정성, 배터리 성능 향상. 그럼에도 불구하고 여전히 리튬-황에 붕소가 첨가된 탄소재료 연구에 있어 많은 문제점 더 많은 연구와 분석이 필요한 배터리입니다. 예를 들어, 영향 붕소 도핑량과 전도성, 표면의 도핑 구성 탄소의 폴리황화리튬의 전하 분포 및 흡착 거동 재료. 동시에 붕소 함량이 높은 탄소재료를 얻는 방법 도핑 수준과 도핑 구성을 정확하게 제어하는 방법은 모두 다릅니다. 첨단 제조 방법 및 기술 개발에 관한 것입니다. ~ 안에 또한 다중 원소 공동 도핑 시스템의 경우 더 적합한 도핑 원소 조합은 아직 더 연구해야 합니다. 체계적인 구축 구조-활동 관계를 통해 시너지 효과 메커니즘을 명확히 합니다. 공동 도핑된 구조와 호스트-게스트의 모드와 강도에 미치는 영향 황 전기화학에서의 상호작용.
2.3 금속붕화물
금속 화합물은 항상 연구 대상이었습니다. 리튬황 배터리 기능성 소재의 핫스팟 본질적인 화학적 극성 특성과 우수한 형태학적 및 구조적 가소성. 일반적인 금속 산화물, 황화물과 다릅니다. 질화물 및 기타 이온 화합물. 금속 붕화물은 일반적으로 붕소로 구성됩니다. 공유 결합을 기반으로 한 금속 원소와 그 채워진 구조는 다음과 같습니다. 금속성의 일부. 다른 금속에 비해 훨씬 높은 전도성을 나타냅니다. 화합물(그림 4)[48, 49, 50, 51, 52, 53, 54, 55, 56]을 제공할 수 있습니다. 전기화학 반응을 위한 전자의 신속한 공급 [57] 동시에, 금속과 붕소 사이에는 국부적으로 제한된 이온 결합 극성 구조가 있습니다. 이는 폴리설파이드에 대한 좋은 흡착 사이트를 제공할 수 있습니다[58,59]. 게다가, 전기음성도가 높은 붕소의 안정성은 다음과 합금화한 후에 약해집니다. 전이 금속이며 산화 환원 반응에 참여하기가 더 쉽습니다. 이것 금속 붕소화물이 리튬-황에 참여할 수 있게 해줍니다. 매개체로서 표면반응을 통한 전기화학적 반응[60].
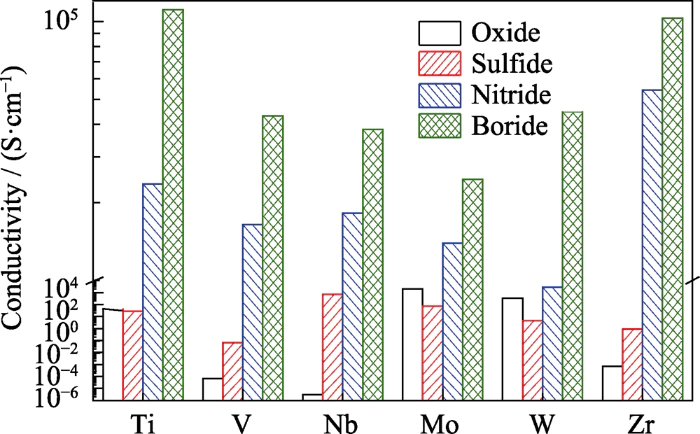
그림. 4 여러 범주의 전도도 비교 금속 화합물[48,49,50,51, 52,53,54,55,56]
Guan et al. [61] 호스트 재료를 준비했다 그래핀에 비정질 Co2B 나노입자를 로딩하여 황 음극을 만드는 방법 액상 환원법. 연구에 따르면 붕소와 코발트 모두 리튬 폴리설파이드를 화학적으로 고정하는 흡착 장소 역할을 할 수 있습니다. 용해 및 이동을 억제합니다. 우수한 장거리 성능과 결합 그래핀의 전도성에도 불구하고 배터리는 여전히 방전 특정 용량을 가지고 있습니다. 1C 속도에서 450사이클 후 758mAh·g-1, 용량 감쇠율은 Cycle은 0.029%로 우수한 Cycle 성능을 나타냅니다. 비슷한 내용을 바탕으로 시너지 흡착 효과가 있는 Co2B@CNT 복합재료를 리튬황전지용 기능성 분리막, 흡착능력 보유 11.67mg·m-2만큼 높은 Li2S6[62] 폴리설파이드의 확산과 침투를 효과적으로 차단하고 셔틀효과를 억제하는 목적. 이를 바탕으로 Guan et al. [63] 또한 2차원 금속탄화물(MXene)을 담체로 사용하여 Co2B@MXene 이종접합 복합재료(그림 5(a~d)). 을 통해 이론적 계산을 통해 전자적 상호작용이 일어나는 것으로 밝혀졌다. 이종접합 인터페이스는 Co2B에서 MXene으로 전자의 이동을 유도합니다. 이 효과는 Co2B의 흡착 및 촉매 능력을 향상시킵니다. 다황화물(그림 5(a, b)). 따라서 용량 감소율은 2000주기 동안 기능적으로 수정된 분리막을 기반으로 하는 Co2B@MXene 배터리 사이클당 0.0088%에 불과합니다. 그리고 5.1mg·cm-2의 황 함량에서도 비용량은 여전히 5.2mAh·cm-2만큼 높습니다(그림 5(c, d)). 와 비교하여 주목해야 할 점은 결정질 상 구조, 이러한 유형의 비정질 상 금속 붕소화물 재료는 재료 준비가 더 부드럽고 간단합니다. 그러나 원자 및 분자 구조의 제어 가능성과 안정성은 상대적으로 열악하여 구성 요소를 명확하게 하는 데 큰 장애물이 됩니다. 미세 구조 및 황에 대한 영향 메커니즘 탐구 전기화학적 반응과정
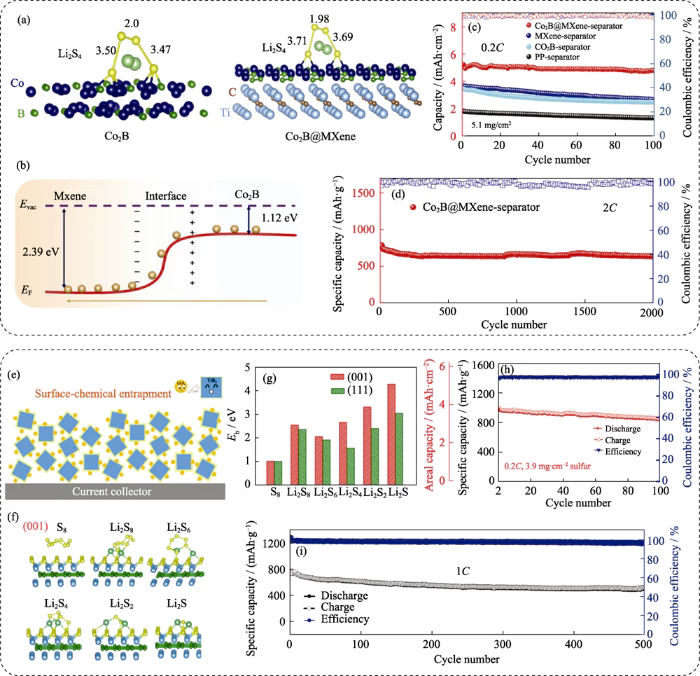
그림. 5 (a) Li2S4 흡착 구성 Co2B 및 Co2B@MXene 표면, (b)에서의 전자 재분배 방식 Co2B와 MXene 사이의 인터페이스, (c) Co2B@MXene 및 기타 분리기를 기반으로 한 전지의 사이클링 성능, (d) Co2B@MXene 전지의 장기 사이클링 성능[63]; (e) 표면 화학적 포착의 개략도 TiB2의 다황화물, (f) 흡착 구성 및 (g) TiB2의 황 종 에너지 TiB2의 (001) 및 (111) 표면, (h) 고부하 성능 및 (i) TiB2 기반 황 전극의 장기 사이클링[63,65]
TiB2는 고전적인 금속 붕소화물입니다. 우수한 전기 전도도(~106 Søcm-1)를 가지며 널리 사용됩니다. 전도성 세라믹, 정밀가공, 전기화학 등의 분야 장치. TiB2는 전형적인 육각형 구조를 가지고 있으며 경도가 높고 구조적 탄력성은 황 반응의 부피 변화에 적응하는 데 도움이 됩니다. 동시에 표면에는 수많은 불포화 구조가 존재합니다. 리튬과 강한 계면 화학적 상호작용을 형성할 것으로 예상됨 폴리설파이드[64]로 인해 우수한 흡착 및 가두기 효과를 얻을 수 있습니다. 리 외. [65]는 TiB2가 황의 호스트 물질로 사용되었다고 처음 보고했습니다. 음극. 그림 5(e~g)와 같이 써멀컴파운딩 공정 중 S를 사용하면 TiB2 표면이 부분적으로 황화됩니다. 리튬폴리설파이드 반응 중에 생성된 물질은 반데르발스(van der Waals)를 통해 효과적으로 흡착됩니다. 힘과 루이스 산-염기 상호작용, 그리고 이 메커니즘의 효과는 다음과 같습니다. (001) 표면에서 더 중요합니다. 획득된 황 음극은 1C 속도에서 500 사이클의 안정적인 사이클과 동시에 특정 100사이클 후에도 용량은 여전히 3.3mAh·cm-2로 유지됩니다. 3.9 mgâcm-2의 유황 함량. 좋은 모습을 보여줬어 전기화학적 성능(그림 5(h, i)). XPS 결과를 바탕으로 분석 및 이론적 계산, 우수한 리튬 폴리설파이드 TiB2의 흡착 효과는 표면에 기인해야 합니다. "패시베이션" 메커니즘. 또한 Lu의 연구 그룹 [66] 리튬 폴리설파이드에 대한 TiB2, TiC 및 TiO2의 흡착 효과 비교 해당 화학 물질 간의 경쟁 메커니즘을 탐색했습니다. 흡착 및 용매화 탈착. 결과는 붕소가 더 낮다는 것을 보여줍니다 전기음성도는 TiB2의 흡착 능력을 더욱 강하게 하며, 용매화 능력이 약한 에테르 전해질을 사용하면 효과적으로 개선될 수 있습니다. 황 활용 및 전기화학 반응의 가역성을 향상시킵니다. 이러한 관점에서 TiB2는 다기능 구성에도 사용되었습니다. 활성 물질을 효율적으로 흡착, 고정 및 재사용하는 분리기 [67] 소재를 사용하여 배터리 사이클 안정성을 크게 향상시켰습니다. 용량 0.5C에서 300사이클 후에도 초기값의 85%를 유지할 수 있습니다.
TiB2와 유사하게 MoB는 전도성이 좋습니다. 그리고 그 본질적인 2차원 구조는 흡착 지점이 형성되어 우수한 황 음극 촉매가 될 것으로 예상됩니다. [68]. 오스틴에 있는 텍사스 대학의 만티람 연구 그룹 [69] Sn을 환원제로 사용하고, 이를 통해 MoB 나노입자를 합성했다. 고체상법으로 우수한 흡착력과 촉매능력을 보여주었다. 리튬폴리설파이드. MoB는 높은 전자 전도도(1.7×105 S…m-1)를 가지며, 이는 황에 대한 전자의 신속한 공급을 제공할 수 있습니다. 반응; 동시에 MoB의 친수성 표면 특성은 다음과 같습니다. 전해질 습윤에 도움이 되며 리튬 이온의 신속한 이동을 돕습니다. 이는 희박 전해질 하에서 활성 물질의 활용을 보장합니다. 정황; 또한 나노 크기의 MoB는 촉매 활성 물질을 완전히 노출시킬 수 있습니다. 전자가 부족한 붕소 원자에 의해 유도된 위치로 인해 재료가 본질적인 촉매 활성과 겉보기 촉매 활성이 모두 우수합니다. 이러한 장점을 바탕으로, MoB를 조금만 첨가해도 성능을 크게 향상시킬 수 있습니다. 전기화학적 성능과 상당한 실용성을 보여줍니다. 결과 배터리는 1,000사이클 이후 사이클당 용량 감쇠가 0.03%에 불과합니다. 1C 속도로. 그리고 황 함량이 3.5mg∙cm-2이고 4.5 mL…g-1의 전해질/황 비율(E/S), 우수한 소프트 패키지 배터리 사이클 성능을 달성했습니다. 또한, Nazar 연구 그룹[70]은 경량 MgB2를 전기화학 물질로 사용했습니다. 리튬 폴리설파이드용 전환 매체. B와 Mg 모두 가능하다는 것이 밝혀졌습니다. 폴리설파이드 음이온의 흡착 부위 역할을 하고, 전자 전달을 강화하며, 높은 황 함유량(9.3mg~cm-2)에서 더 나은 순환 안정성을 달성합니다.
이 작품들은 황 개선에 있어 금속 붕화물의 효과 및 우수성 전기화학 반응. 그러나 금속 산화물과 같은 시스템에 비해 및 황화물에 대한 금속 붕화물에 대한 연구 보고서는 아직 상대적으로 적습니다. 리튬-황 배터리 소재 및 관련 메커니즘 연구 또한 확대되고 심화되어야 한다. 또한, 결정성 금속 붕화물 일반적으로 구조적 강도가 높으며 준비 과정에 높은 에너지 장벽을 넘어 고온, 고압 및 기타 가혹한 조건으로 인해 연구 및 적용이 제한됩니다. 그러므로, 간단하고 온화하며 효율적인 금속붕소 합성법 개발 금속붕화물 연구에서도 중요한 방향이다.
2.4 비금속붕화물
금속 붕소화물에 비해 비금속 붕화물은 일반적으로 밀도가 낮고 가볍기 때문에 고에너지밀도 배터리 개발; 그러나 전도성이 낮습니다. 황 전기화학의 효율성과 동역학에 대한 저항을 생성합니다. 반응. 현재 연구자들은 건설 분야에서 일정한 진전을 이루었습니다. 비금속 붕소화물을 기반으로 한 리튬-황 배터리용 황 고정 소재 질화붕소, 탄화붕소, 인화붕소, 황화붕소를 포함[71, 72, 73].
질화붕소(BN) 및 탄화붕소(BC) 가장 대표적이고 널리 연구된 두 가지 비금속 붕소화물입니다. BN은 질소 원자와 붕소 원자가 교대로 연결된 구조로 이루어져 있으며, 주로 육각형, 삼각형, 입방형 및 백류석의 네 가지 결정 형태를 포함합니다[74]. 중에 그 중 육방정계 질화붕소(h-BN)는 폭이 넓은 특성을 나타냅니다. 밴드갭, 높은 열 전도성, 우수한 열적, 화학적 안정성 흑연과 같은 2차원 구조와 국부적인 전자 분극 특성 [75,76] . B-N 구조는 분명한 극성 특성을 가지고 있습니다. 폴리황화리튬에 대한 강력한 화학적 흡착 능력을 가지고 있습니다. 에서 동시에 표면의 화학적 특성을 제어할 수 있습니다. 안정성을 보장하기 위해 요소 도핑 및 토폴로지 결함 구성 흡착 강도를 향상시키면서 폴리설파이드 분자 구조 [77]. 이 아이디어를 바탕으로 Yi et al. [78]은 질소가 부족한 소수 층을 보고했습니다. 황 음극용 호스트 재료인 질화붕소(v-BN)(그림 6(a)). 연구에 따르면 v-BN의 전기양성 공석은 다음과 같은 도움이 될 뿐만 아니라 폴리설파이드를 고정하고 변환할 뿐만 아니라 확산과 이동을 가속화합니다. 리튬 이온의. 원래 BN과 비교하여 v-BN 기반 음극은 더 높습니다. 초기 용량은 0.1C(1262 vs 775mAh·g-1), 용량은 1C에서 500회 주기 후 붕괴율은 주기당 0.084%에 불과합니다. 좋은 모습을 보여줌 사이클링 안정성. 또한 He et al. [79] O 도핑이 더 많은 것을 가능하게 한다는 것을 발견했습니다. BN 표면의 화학적 극성을 개선하고 물질이 형성되도록 유도합니다. 더 큰 비표면적과 동시에 고유성과 겉보기 흡착 특성.
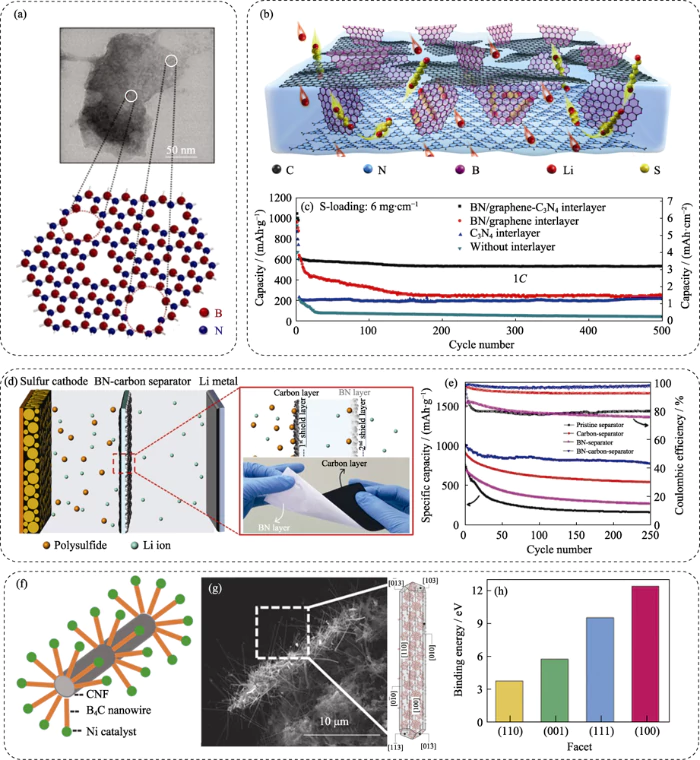
그림. 6 (a) TEM 이미지 및 개략적인 원자 구조 v-BN[78]; (b) g-C3N4/BN/그래핀 복합 이온체의 계획 및 (c) 상응하는 Li-S 전지 사이클링 성능[80]; (d) BN/Celgard/탄소 삼중층 분리막의 도식 및 광학 이미지, (e) 상응하는 세포 순환 성능; (f) B4C@CNF의 계획 및 (g) SEM 이미지와 B4C 나노와이어 모델, (h) Li2S4 흡착 에너지 B4C의 다양한 측면[87]
BN 소재는 화학적 성질이 좋지만 흡착 특성, 자체 전도성이 좋지 않아 반응성에 도움이 되지 않습니다. 요금 이체. 따라서 전도성을 지닌 복합구조물의 설계는 재료는 포괄적인 흡착을 더욱 향상시키는 중요한 방법입니다. 및 촉매 성능. 이를 고려하여 Deng et al. [80] 디자인했다 흑연형 질화탄소(g-C3N4), BN 및 리튬-황 배터리용 다기능 중간층인 그래핀 (그림 6(b)). 그 중 g-C3N4에 있는 0.3 nm 크기의 정렬된 이온 채널은 구조는 다황화물을 효과적으로 차단하고 리튬 이온을 통과시킬 수 있습니다. 을 통해. BN은 반응 촉매 역할을 하여 전환을 촉진합니다. 폴리설파이드, 그래핀이 내장된 집전체 역할을 하여 우수한 장거리 전도성. . 이들의 시너지 효과 덕분에 3개의 2차원 구성 요소로 인해 생성된 배터리는 안정적으로 순환할 수 있습니다. 6mg·cm-2의 높은 황 함량과 1C의 속도에서 500사이클 이상.(그림 6(c)) 또한, 연구자들은 BN 나노시트/그래핀 복합 필름의 얇은 층을 적용하려고 시도했습니다. 보다 간단하고 직접적인 형태로 음극 표면을 보호층으로 사용 [81,82]. 리튬의 용해 및 확산을 효과적으로 억제합니다. 폴리설파이드를 함유하고 비용량과 사이클을 크게 향상시킵니다. 황 음극의 안정성. 3C에서 1000주기 동안 용량은 감쇠율은 사이클당 0.0037%에 불과합니다. 흥미롭게도 백운규는 한양대학교 연구진[83]은 또 다른 아이디어 조합을 채택했다. BN/Celgard/카본 샌드위치를 이용한 다기능 분리막 제작 구조. 그림 6(d)와 같이 탄소층과 BN층은 양극과 음극 면에 각각 코팅되어 있습니다. 일반 분리기. 그 중 탄소층과 BN층이 결합할 수 있다. 폴리황화리튬의 셔틀을 차단하고 표면으로의 확산을 제한합니다. 음극의. 동시에 네거티브의 BN층 전극 측은 또한 리튬 수상돌기의 성장을 제한합니다. 덕분에 협력적인 보호 메커니즘으로 배터리의 용량 유지력이 높습니다. 전송률(76.6%) 및 비용량(780.7mAh…g-1) 0.5C에서 250사이클 후. 일반 분리막에 비해 월등히 우수하며, 순수 탄소 개질 분리막(그림 6(e))
N에 비해 C는 더 낮습니다. 전기음성도이므로 B와 C의 전기음성도 차이는 다음과 같습니다. 작아서 B-C 구조의 화학적 극성이 약해집니다. NC. 그러나 동시에 B-C 구조의 전자 비편재화는 다음과 같습니다. 강화되고 전도도가 더 좋습니다[84,85]. 따라서 BC는 일반적으로 BN과 상대적으로 보완적인 물리적, 화학적 특성. 낮은 밀도, 상대적으로 좋은 전도성, 좋은 촉매 특성을 가지고 있습니다. 에너지 분야에서 유망한 응용 전망을 갖고 있다[86]. Luoet al. [87] 성장했다 음극 호스트로서 탄소 섬유에 있는 탄화붕소 나노와이어(B4C@CNF) 재료(그림 6(f~h)). 그 중 B4C는 효율적으로 흡착하고 가두는 역할을 합니다. B-S 결합을 통한 다황화물. 동시에, 탄소 섬유 전도성 네트워크는 흡착된 황의 빠른 전환을 돕고 반응을 향상시킵니다. 동력학. 획득된 황 음극은 500°C 이후 80%의 용량 유지율을 갖는다. 높은 황 함량(질량 분율) 하에서 안정적인 순환을 달성할 수 있습니다. 70%) 및 적재 용량(10.3 mg…cm-2). Songet al. [88] B4C 주변에 초밀폐 황 호스트 구조를 구축했습니다. 구조 유연한 매트릭스 B4C로 활성 다공성 면직물 탄소를 사용합니다. 나노섬유를 활성골격으로 하고, 환원그래핀옥사이드를 추가로 사용한다. 코팅. 물리적, 화학적 구속을 효율적으로 결합하여 유효성분의 손실이 적고, 우수한 사이클 안정성을 달성합니다. 을 고려하여 Zhao의 연구 그룹인 B4C의 우수한 흡착 및 촉매 특성 [89] B4C 나노입자를 탄소섬유 천에 균일하게 분포 효율적으로 분산 및 노출시키는 in-situ 촉매 보조 성장 방법 활성 사이트. 얻은 황 음극은 최대 1415의 초기 용량을 갖습니다. 3.0mg·cm-2 로딩 시 mAh·g-1(0.1C) 및 1C에서 3000사이클의 매우 긴 수명을 가지며, 좋은 응용 가능성을 보여줍니다.
위에서 알 수 있듯이 비금속 붕화물은 리튬에 대한 흡착 및 촉매 효과가 우수합니다. 다황화물이지만 전도성이 상대적으로 낮고 전도성 담체입니다. 황 전기화학 반응을 돕기 위해서는 여전히 필요합니다. 그 중에는 인접한 N 및 C 원자의 전자 구조의 차이로 인해 BN이 생성되고 BC 소재는 장점과 단점이 있습니다. 전도성 및 리튬폴리설파이드와의 상호작용. 이를 고려하여, 황화 붕소, 인화 붕소, 산화 붕소 등과 결합하여 이러한 유형의 비금속 붕소화물은 좋은 캐리어와 플랫폼으로 사용될 수 있습니다. 국소적인 화학적 극성 구조와 구조-활성 관계 흡착촉매능력. 더욱 체계화될 것으로 예상됩니다. 상관관계 및 분석은 관련 미세 반응을 이해하는 데 도움이 됩니다. 공정을 조절하고, 재료의 미세 구조를 조절하고, 배터리의 전기화학적 성능. 또한, 추가 응용 프로그램 리튬-황 배터리의 비금속 붕소화물 개발은 여전히 필요합니다. 준비의 개선과 최적화에 의존합니다. 간단한 개발 온화한 준비 기술을 사용하여 재료 구조를 개발하는 동시에 더 높은 고유 전도성 및 보다 효율적인 복합 재료 설계 전도도, 흡착 및 촉매의 균형을 맞추고 고려합니다. 효과.
3 결론
요약하면 리튬황 배터리는 다중 전자 전달 반응으로 인해 높은 이론적 에너지 밀도. 그러나 그들의 전환 반응 메커니즘과 본질적인 취약성은 활물질의 전도성은 장점의 실현을 방해합니다. 붕소계 소재는 독특한 물리적, 화학적 특성을 가지고 있으며, 전기화학적 특성. 그들의 타겟 디자인과 합리적인 적용은 리튬-황 배터리의 셔틀 효과를 완화하는 효과적인 방법과 반응 역학 및 가역성을 향상시킵니다. 그들은 급속도로 발전해 왔습니다. 최근 몇 년. 그러나 붕소 기반 물질의 연구 및 응용은 리튬-황 배터리는 아직 초기 단계이며, 재료 구조는 배터리 전기화학 반응에 대한 설계 및 작용 메커니즘 프로세스를 더욱 개발하고 탐색해야 합니다. 재료를 결합 이러한 특징과 위의 연구 진행 상황을 통해 저자는 리튬-황 배터리의 향후 붕소 기반 소재 개발은 다음 지침에 더 주의를 기울이십시오:
1) 물질 합성. 인조 준비는 위에서 언급한 붕소 기반 제조 공정이 직면하는 일반적인 문제입니다. 재료. 더 단순하고, 더 온화하고, 더 많은 개발이 시급합니다. 메커니즘의 재료 기반을 제공하는 효율적인 재료 준비 방법 연구 및 응용 프로그램 홍보. 그 중 무정형의 제조 액상환원법에 의한 금속붕소화물은 유망한 개발이다 방향. 동시에, 그 장점과 경험을 활용하여, 용매열 또는 용융염을 기반으로 한 합성 경로 탐색 및 개발 방법은 또한 붕소 기반의 제조에 대한 새로운 아이디어를 제공할 수도 있습니다. 재료. 또한, 붕화물 제조 과정에서 특수한 나노구조의 제어와 설계에 주의를 기울여야 하며, 인터페이스 반응 특성의 요구를 충족시키는 안정성 리튬-황 배터리.
2) 메커니즘 탐구. 붕소 기반 재료는 독특하고 풍부한 표면 화학적 특성을 가지고 있습니다. 현장 호스트-게스트를 추가로 연구하려면 특성화 방법을 사용해야 합니다. 붕소 기반 물질과 다황화물 간의 상호 작용. 특별한 관심 돌이킬 수 없는 황산화, 자기 전기화학적 표면을 처리해야 합니다. 산화, 환원 등을 통해 결정적인 구조적 요인을 밝힙니다. 흡착 및 촉매 기능을 제공하고 이론적 지침을 제공하며 재료의 목표 설계 및 개발을 위한 기반. 또한, 대표적인 비정질 금속 붕소화물은 별도의 비용을 지불해야 합니다. 미세 구조 및 관련 물리적, 비정질과 결정질 붕소화물 사이의 화학적 성질과 협력 해당 구조해석 및 특성의 개발로 특성화 분석 기술. 간의 상호작용을 추론하지 마세요. 비정질 물질, 리튬 폴리설파이드 및 그 반응 공정만을 기반으로 함 결정 구조에 관한 것입니다.
3) 성과평가. 최적화하려면 소재 및 배터리 평가 시스템, 유황 표면 증가 로딩과 같은 주요 매개변수를 규제하는 데 더 많은 주의를 기울여야 합니다. 전극의 두께와 기공률을 동시에 향상시켜 품질을 향상시킵니다. 전극의 체적 에너지 밀도. 또한, 낮은 전해질 투여량(E/S<5 mL…g-1S) 및 낮은 음극/양극 용량 비율(N/P<2) 조건에서 전기화학적 특성을 추가로 조사했습니다. 동시에 실험실용 버튼 셀부터 원통형 또는 연포장 배터리의 실제 생산까지 증폭 효과와 관련 과학 및 엔지니어링 문제를 탐구하고, 배터리 수준의 성능 경쟁력을 합리적이고 종합적으로 평가합니다. 리튬-황 전지의 상업적 개발을 위한 지침 및 참고자료를 제공한다.
요약하자면, 이 기사는 다음에 중점을 두고 있습니다. 붕소 기반 소재를 소개하고 보로펜의 최신 연구 진행 상황을 검토하고, 붕소 원자가 도핑된 탄소, 리튬-황의 금속 붕화물 및 비금속 붕화물 배터리 시스템. 동료들에게 참고와 영감을 줄 수 있기를 바라며, 붕소계 소재 개발 및 응용 분야 확대 새로운 에너지를 제공하고 리튬황전지의 실용화를 촉진한다.
참고자료
[1] DUNN B, KAMATH H, TARASCON J M. 그리드용 전기 에너지 저장: 선택의 여지가 있는 배터리입니다. 과학, 2011,334(6058):928-935.
[2] ARICO AS, BRUCE P, SCROSATI B, et al. 첨단 에너지 변환 및 저장 장치를 위한 나노구조 소재. 자연재료, 2005,4(5):366-377.
[3] LIANG Y R, ZHAO C Z, YUAN H, et al. 에이 휴대용 전자기기용 2차 전지에 대한 검토입니다. 정보매트, 2019,1(1):6-32.
[4] GOODENOUGH JB, PARK K S. 리튬 이온 충전식 배터리: 관점. 미국 화학 학회지, 2013,135(4):1167-1176.
[5] TARASCON J M, ARMAND M. 문제 및 충전식 리튬 배터리가 직면한 과제. 자연, 2011,414:171-179.
[6] JING Y, HE HC, WU J, et al. 리튬 음극용 황 호스트로서 코발트가 도핑된 중공 탄소 골격 유황 배터리. 무기재료학회지, 2021,36(2):203-209.
[7] FANG R, ZHAO SY, SUN Z H, et al. 더 신뢰할 수 있는 리튬-황 배터리: 상태, 솔루션 및 전망. 고급의 자료, 2017,29(48):1606823.
[8] HU J J, LI GR, GAO X P. 현재 리튬-황 배터리의 현황, 문제점 및 과제. 저널 무기재료, 2013,28(11):1181-1186.
[9] LI GR, WANG S, ZHANG Y N, et al. 리튬-황 배터리에서 다황화물의 역할을 재검토합니다. 고급의 자료, 2018,30(22):1705590.
[10] PENG H J, HUANG J Q, ZHANG Q. 리뷰 유연한 리튬-황 및 유사한 알칼리 금속-칼코겐 충전식 배터리. 화학회평론, 2017,46(17):5237-5288.
[11] JANA M, XU R, CHENG X B, et al. 리튬-황 배터리용 2차원 나노소재의 합리적 설계. 에너지환경과학, 2020,13(4):1049-1075.
[12] HE J R, MANTHIRAM A. 리튬-황 배터리 전기촉매의 현황과 과제. 에너지 저장재료, 2019,20:55-70.
[13] SEH Z W, SUN Y M, ZHANG Q F, et al. 고에너지 리튬-황 배터리 설계. 화학 학회 리뷰, 2016,45(20):5605-5634.
[14] JI X L, EVERS S, BLACK R, et al. 폴리황화물 저장소를 사용하여 리튬-황 음극을 안정화합니다. 자연 커뮤니케이션, 2011,2:325.
[15] ZHANG Z, KONG L L, LIU S, 외. 에이 3D 그래핀 나노시트@탄소 기반 고효율 황/탄소 복합재 리튬-황 배터리용 음극으로 사용되는 나노튜브 매트릭스. 첨단에너지 자료, 2017,7(11):1602543.
[16] XU W C, PAN X X, MENG X, et al. 에이 초미립자 질화바나듐을 함유한 전도성 황 함유 물질 고성능 리튬-황 배터리용 나노입자. 일렉트로키미카 액타, 2020,331:135287.
[17] LIU Y T, LIU S, LI GR, et al. 높은 중금속 및 촉매 금속 산화물을 포함하는 체적 에너지 밀도 황 음극 리튬-황 배터리용 호스트. 첨단과학, 2020,7(12):1903693.
[18] CHEN H H, XIAO Y W, CHEN C, et al. 리튬-셔틀 효과를 완화하기 위한 전도성 MOF 변형 분리막 여과 방식을 통한 유황 배터리. ACS 응용 재료 & 인터페이스, 2019,11(12):11459-11465.
[19] YOO J, CHO S J, JUNG G Y, et al. 분자적으로 설계된 계층적 다공성 화학 트랩인 CNT-net의 COF-net 리튬-황 배터리의 다황화물용. 나노문자, 2016,16(5):3292-3300.
[20] HU Y, LIU C. 소개 유기붕소 화합물의 1,2-이동. 대학 화학, 2019,34(12):39-44.
[21] SOREN KM, SUNING W. 보론계 자극 반응 물질. 화학회 리뷰, 2019,48(13):3537-3549.
[22] HUANG Z G, WANG SN, DEWHURST R D 등 알. 붕소: 에너지 관련 공정 및 응용 분야에서의 역할. 안게반테 Chemie International Edition, 2020,59(23):8800-8816.
[23] ZHU YH, GAO S M, HOSMANE N S. 붕소가 풍부한 첨단 에너지 소재. 무기질 치미카 액타, 2017,471:577-586.
[24]KHAN K, TAREEN AK, ASLAM M, et al. 의 합성, 특성 및 새로운 전기촉매 응용 2D-보로펜 크센. 고체 화학의 발전, 2020,59:100283.
[25] RAO D W, LIU X J, YANG H 등. 보로펜 기반 양극과 전해질 간의 계면 경쟁 리튬황 배터리의 다중 황화물 고정화. 저널 재료화학A, 2019,7(12):7092-7098.
[26] JIANG HR, SHYY W, LIU M, et al. 잠재적인 고정 재료로서의 보로펜 및 결함 보로펜 리튬-황 배터리: 첫 번째 원리 연구. 재료 저널 화학A, 2018,6(5):2107-2114.
[27] ZHANG CY, HE Q, CHU W, et al. 견고성을 위한 전이 금속 도핑된 보로펜-그래핀 헤테로구조 다황화물 고정: 첫 번째 원리 연구. 응용표면과학, 2020,534:147575.
[28] ZHANG L, LIANG P, SHU H B, et al. 리튬-황 배터리를 위한 효율적인 황 호스트로서의 보로펜: 억제 셔틀 효과 및 전도성 향상. 물리화학 저널 C, 2017,121(29):15549-15555.
[29] GRIXTI S, MUKHERJEE S, SINGH C V. 인상적인 리튬-황 배터리 음극으로서의 2차원 붕소 재료. 에너지저장재료, 2018,13:80-87.
[30] MANNIX AJ, ZHOU X F, KIRALY B, et al. 보로펜의 합성: 이방성, 2차원 붕소 다형체. 과학, 2015,350(6267):1513-1516.
[31] FENG B J, ZHANG J, ZHONG Q, et al. 2차원 붕소 시트의 실험적 구현. 자연화학, 2016,8(6):564-569.
[32] PARAKNOWITSCH J P, THOMAS A. 도핑 질소 너머의 탄소: 고급 헤테로원자 도핑 탄소에 대한 개요 에너지 응용 분야를 위한 붕소, 황 및 인. 에너지 & 환경과학, 2013,6(10):2839-2855.
[33] WANG H B, MAIYALAGAN T, WANG X. 리뷰 질소 도핑 그래핀의 최근 진행 상황: 합성, 특성화 및 그것의 잠재적인 응용. ACS 촉매작용, 2012,2(5):781-794.
[34] XIE Y, MENG Z, CAI TW, et al. 효과 리튬황의 음극으로 사용되는 그래핀 에어로겔에 붕소 도핑 배터리. ACS 응용재료 및 인터페이스, 2015,7(45):25202-25210.
[35] SHI PC, WANG Y, LIANG X, et al. 황을 캡슐화하기 위해 동시에 박리된 붕소 도핑 그래핀 시트 리튬-황 배터리에 적용됩니다. ACS 지속 가능한 화학 및 공학, 2018,6(8):9661-9670.
[36] YANG L J, JIANG S J, ZHAO Y, et al. 산소를 위한 금속이 없는 전기촉매로서 붕소가 첨가된 탄소 나노튜브 환원 반응. Angewandte Chemie 국제판, 2011,50(31):7132-7135.
AI W, LI J W, DU Z Z, et al. 듀얼 붕소 도핑된 다공성 탄소 구/그래핀 하이브리드에 다황화물을 가두는 방법 고급 Li-S 배터리용. 나노연구, 2018,11(9):4562-4573.
[38] YANG C P, YIN Y X, YE H, et al. 황/탄소 음극에 대한 붕소 도핑 효과에 대한 통찰력 리튬-황 배터리. ACS 응용 재료 및 인터페이스, 2014,6(11):8789-8795.
[39] XU C X, ZHOU H H, FU C P, 외. 붕소 도핑된 압축 해제된 탄소 나노튜브/황의 열수 합성 고성능 리튬-황 배터리용 복합재. 일렉트로키미카 액타, 2017,232:156-163.
[40] HAN P, MANTHIRAM A. Boron- 및 고성능을 위한 질소 도핑 환원 그래핀 산화물 코팅 분리막 Li-S 배터리. 전원저널, 2017,369:87-94.
[41] HOU T Z, CHEN X, PENG H J, et al. 강력한 고정을 달성하기 위한 헤테로원자 도핑 나노탄소의 설계 원리 리튬-황 배터리용 다황화물. 소, 2016,12(24):3283-3291.
[42] XIONG D G, ZHANG Z, HUANG XY, et al. B/N-코도핑된 계층적 다공성에서 다황화물 감금 강화 안정적인 Li-S 배터리를 위한 루이스 산-염기 상호작용을 통한 탄소 나노시트. 에너지화학저널, 2020,51:90-100.
[43] YUAN SY, BAO J L, WANG L N, 외. 향상된 그래핀 지지 질소 및 붕소가 풍부한 탄소층 향상된 화학 흡착으로 인해 리튬-황 배터리의 성능이 향상되었습니다. 리튬 폴리설파이드. 첨단에너지재료, 2016,6(5):1501733.
[44] CHEN L, FENG J R, ZHOU H H, et al. 질소, 붕소 공동 도핑 곡선형 그래핀의 열수 제조 고성능 리튬황을 위한 높은 도펀트 양의 나노리본 배터리 음극. Journal of Materials Chemistry A, 2017,5(16):7403-7415.
[45] JIN C B, ZHANG W K, ZHUANG Z Z, et al. 붕소와 산소가 이중으로 도핑된 다중벽을 사용하여 향상된 황화물 화학흡착 첨단 리튬-황 배터리용 탄소나노튜브. 재료 저널 화학A, 2017,5(2):632-640.
[46] ULLAH S, DENIS PA, SATO F. 특이한 나트륨과 칼륨의 흡착 에너지 강화 황-질소 및 규소-붕소 공동도핑된 그래핀. ACS 오메가, 2018,3(11):15821-15828.
[47] ZHANG Z, XIONG D G, SHAO A H, 외. 금속성 코발트 및 N/B 헤테로원자를 다공성 탄소 나노시트에 통합 리튬-황 배터리를 위한 효율적인 황 고정 장치입니다. 탄소, 2020,167:918-929.
[48] WANG P, KUMAR R, SANKARAN EM, et al. 고압에서 합성된 이붕화바나듐(VB2): 탄성, 기계적, 전자 및 자기 특성과 열 안정성. 무기화학, 2018,57(3):1096-1105.
HE G J, LING M, HAN XY, et al. 고성능을 위한 코어-쉘 구조의 자립형 전극 슈퍼커패시터. 에너지저장재료, 2017,9:119-125.
[50] WANG C C, AKBAR SA, CHEN W, et al. 고온 산화물, 붕화물, 탄화물 및 질화물. 재료과학저널, 1995,30(7):1627-1641.
[51] XIAO Z B, YANG Z, ZHANG L J, et al. 고황함유, 초고속화를 위한 샌드위치형 NbS2@S@I 도핑 그래핀 그리고 수명이 긴 리튬황 배터리. ACS Nano, 2017,11(8):8488-8498.
[52] WANG L J, LIU F H, ZHAO BY, 외. MoS2 나노시트를 전극재료로 채운 탄소나노보울 슈퍼커패시터. ACS 응용나노재료, 2020,3(7):6448-6459.
[53] BALACH J, LINNEMANN J, JAUMANN T 등 알. 첨단 리튬-황 배터리용 금속 기반 나노구조 소재. Journal of Materials Chemistry A, 2018,6(46):23127-23168.
[54] 벤도르 엘, 쉬모니 Y. 크리스탈 순수의 구조, 자화율 및 전기 전도성 NiO 도핑된 MoO2 및 WO2. 재료연구회보, 1974,9(6):837-44.
[55] SAMSONOV G. é¼çååç©æå. å京:ä¸å½å·¥ä¸åºç礼, 1965: 1-147.
FENG LS, QUN C X, LIN M Y, et al. 리튬이온 배터리용 양극재로 사용되는 Nb 기반 산화물. 진행 상황 화학, 2015,27(2/3):297-309.
TAO Q, MA SL, CUI T, et al. 기능성 전이금속 붕소화물의 구조와 특성. 액타 피지카 Sinica, 2017,66(3):036103.
[58] SHEN Y F, XU C, HUANG M, et al. 붕소 클러스터, 보란 및 금속 도핑 붕소 화합물의 연구 발전. 화학진보, 2016,28(11):1601-1614.
[59] GUPTA S, PATEL M K, MIOTELLO A, et al. 전기화학적 물 분해를 위한 금속 붕화물 기반 촉매: 검토. 첨단기능재료, 2020,30(1):1906481.
[60] WU F, WU C. 신규 이차전지 다중전자반응 개념을 바탕으로 핵심소재를 연구하고 있습니다. 중국과학공보, 2014,59(27):3369-3376.
GUAN B, FAN LS, WUX, et al. 그만큼 손쉬운 합성과 강화된 리튬-황 배터리 성능 비정질 코발트 붕화물(Co2B)@그래핀 복합 음극. 재료 저널 화학A, 2018,6(47):24045-24049.
GUAN B, ZHANG Y, FAN LS, et al. Co2B@CNT로 '상승적 흡착 효과'를 통해 다황화물 차단 초고속 성능과 견고한 리튬-황 배터리. ACS나노, 2019,13(6):6742-6750.
[63] GUAN B, SUN X, ZHANG Y 등. 그만큼 코발트 붕소화물@MXene 내 계면 전자 상호작용 발견 고성능 리튬-황 배터리. 중국 화학 편지, 2020,32(7):2249-2253.
[64] BASU B, RAJU GSURI A. 가공 및 모놀리식 TiB2 기반 재료의 특성. 국제 자료 리뷰, 2006,51(6):352-374.
LI C C, LIU X B, ZHU L, et al. 고급 황 호스트로서 전도성 및 극성 티타늄 붕소화물 리튬-황 배터리. 재료화학, 2018,30(20):6969-6977.
[66] LI Z J, JIANG HR, LAI NC, et al. 촉매 황 전환을 위한 효과적인 용매-촉매 인터페이스 설계 리튬-황 배터리에서. 재료공학, 2019,31(24):10186-10196.
[67] JIN L M, NI J, SHEN C, et al. 다기능 분리막 개질제로서의 금속 전도성 TiB2 개선된 리튬황 배터리. 전원 저널, 2020,448:227336.
[68] WUR, XU H K, ZHAO Y W, 외. MoB2의 보로펜 유사 붕소 하위 단위 삽입 몰리브덴 프레임워크는 다음을 가능하게 합니다. 안정적이고 빠르게 작동하는 Li2S6 기반 리튬-황 배터리. 에너지 저장 자료, 2020,32:216-224.
[69] HE JR, BHARGAV A, MANTHIRAM A. 폴리황화물 산화환원을 위한 효율적인 촉매로서의 몰리브덴 붕화물 고에너지 밀도 리튬-황 배터리. 첨단재료, 2020,32(40):2004741.
[70] PANG Q, KWOK CY, KUNDU D, et al. 경량 금속 MgB2는 폴리황화물 산화환원을 중재하고 약속합니다. 고에너지 밀도 리튬-황 배터리. Joule, 2019,3(1):136-148.
[71] YU T T, GAO P F, ZHANG Y, et al. 리튬-황의 잠재적 고정 물질인 인화붕소 단층 배터리: 첫 번째 원리 연구. 응용표면과학, 2019,486:281-286.
[72] JANA S, THOMAS S, LEE C H, et al. B3S 단층: 리튬이온용 고성능 음극재 예측 배터리. Journal of Materials Chemistry A, 2019,7(20):12706-12712.
[73] SUN C, HAI C X, ZHOU Y 등. 고도로 전처리된 케첸블랙에서 성장한 촉매 질화붕소 나노섬유 리튬황 배터리 성능 향상을 위한 양극재. ACS 적용 에너지재료, 2020,3(11):10841-10853.
[74] ARENAL R, 로페즈 베자닐라 A. 보론 질화물 재료: 0D에서 3D(나노)구조까지의 개요. 와일리 학제간논평-전산분자과학, 2015,5(4):299-309.
JIANG X F, WENG Q H, WANG X B, et al. 질화붕소의 제조 및 응용에 관한 최근 진전 나노재료: 리뷰. 재료 과학 및 기술 저널, 2015,31(6):589-598.
[76] PRAKASH A, NEHATE S D, SUNDARAM K B. 열악한 환경을 위한 질화붕소 기반 금속-절연체-금속 UV 검출기 환경 응용 프로그램. 광학편지, 2016,41(18):4249-4252.
[77] ZHAO Y M, YANG L, ZHAO J X, et al. 어떻게 불활성 질화붕소 나노시트를 활성화하여 고정화합니다. 리튬-황 배터리용 다황화물: 전산 연구. 물리적 화학화학물리학, 2017,19(28):18208-18216.
[646][78] YI Y K, LI HP, CHANG H H, et al. 촉진을 위해 가공된 질소 공극을 갖는 소수층 질화붕소 리튬-황 배터리용 양극 매트릭스로서 폴리설파이드의 전환. 화학, 2019,25(34):8112-8117.
HE B, LI W C, ZHANG Y, et al. 파라제네시스(Paragenesis) BN/CNT는 높은 속도 및 매우 긴 수명의 리튬-황 배터리. 재료화학 저널 A, 2018,6(47):24194-24200.
[80] DENG DR, BAI CD, XUE F, et al. Li-S용 중간층으로 2차원 소재로 구성된 다기능 이온체 배터리. ACS 응용재료 및 인터페이스, 2019,11(12):11474-11480.
[81] SUN K, GUO P Q, SHANG X N, 외. 효율적인 메조다공성 질화붕소/그래핀 변형 분리막 매우 안정적인 리튬-황 배터리를 위한 다황화물 장벽. 저널 전기분석화학, 2019,842:34-40.
FAN Y, YANG Z, HUA W X, et al. 빠른 속도와 빠른 속도를 위한 기능화된 질화붕소 나노시트/그래핀 중간층 수명이 긴 리튬-황 배터리. 첨단에너지소재, 2017,7(13):1602380.
[83] KIM PJH, SEO J, FU K, et al. 안정성이 뛰어난 BN-탄소 분리막의 시너지 보호 효과 리튬황 배터리. NPG 아시아 재료, 2017,9(4):e375.
[84] PRAMANICK A, DEY PP, DAS P K. 스파크 플라즈마의 미세 구조, 위상 및 전기 전도도 분석 WEDM으로 가공된 소결 붕소 탄화물. 세라믹스 인터내셔널, 2020,46(3):2887-2894.
[85] YEGANEH M, SARAF H H, KAFI F, et al. 진동, 전자 및 광학의 첫 번째 원리 조사 그래핀과 유사한 탄화붕소의 특성. 솔리드 스테이트 통신, 2020,305:113750.
[86] CHANG Y K, SUN X H, MA M D, 외. 에너지 저장에 경질 세라믹 소재 B4C 적용: 디자인 B4C@C 유연한 전고체 마이크로-전극을 위한 전극으로서의 코어-쉘 나노입자 매우 높은 순환성을 지닌 슈퍼커패시터. 나노에너지, 2020,75:104947.
[87] LUO L, CHUNG SH, ASL HY, et al. 이중 기능성 음극 기판을 갖춘 장수명 리튬-황 배터리 탄화붕소 나노와이어로 구성되었습니다. 첨단재료, 2018,30(39):1804149.
[88] SONG N N, GAO Z, ZHANG Y Y, et al. B4C 나노골격이 가능한 유연한 리튬-황 배터리. 나노에너지, 2019,58:30-39.
[89] ZHANG R H, CHI C, WU M C, et al. 에이 B4C가 잘 분포된 음극으로 수명이 긴 Li-S 배터리 나노입자로 장식된 활성 면 섬유. 전원 저널, 2020,451:227751.



